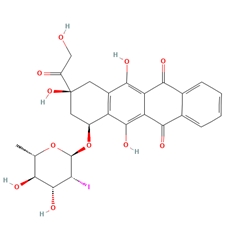
与第一代蒽环类抗肿瘤药物多柔比星(Doxorubicin)相比,Annamycin无明显的心脏毒性。
结构:
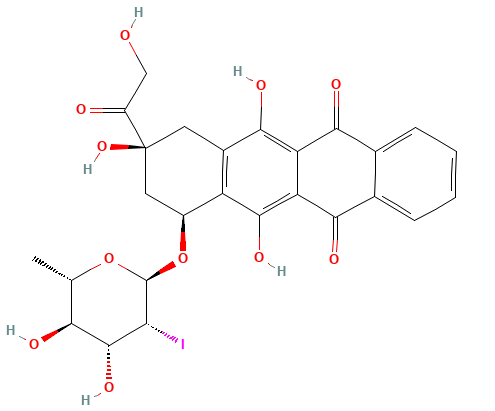
介绍:
Annamycin是美国德克萨斯大学安德森癌症研究中心(The University of Texas MD Anderson Cancer Center)于90的年代开发的蒽环类抗肿瘤药物。目前由Moleculin Biotech进行商业开发。
蒽环类药物能够插入肿瘤DNA,阻止DNA复制,并能够抑制Ⅱ型DNA拓扑异构酶,阻止DNA正常解旋,蒽环类分子结构的醌部分,还通过产生活性氧发挥细胞毒性作用。
影响蒽环类药物临床应用的主要是原发性与获得性多药耐药(MDR)及心脏毒性。脂质体制剂,可以减少药物在心肌暴露量。由于肿瘤血管的通透性增强,脂质体更容易到达肿瘤,而肿瘤易发生淋巴回流受阻,有助于脂质体在肿瘤内富集。第一代蒽环类抗肿瘤药物多柔比星(Doxorubicin),由于亲脂性有限,主要分布于脂质体中心的水相,脂质体的载药量受限。
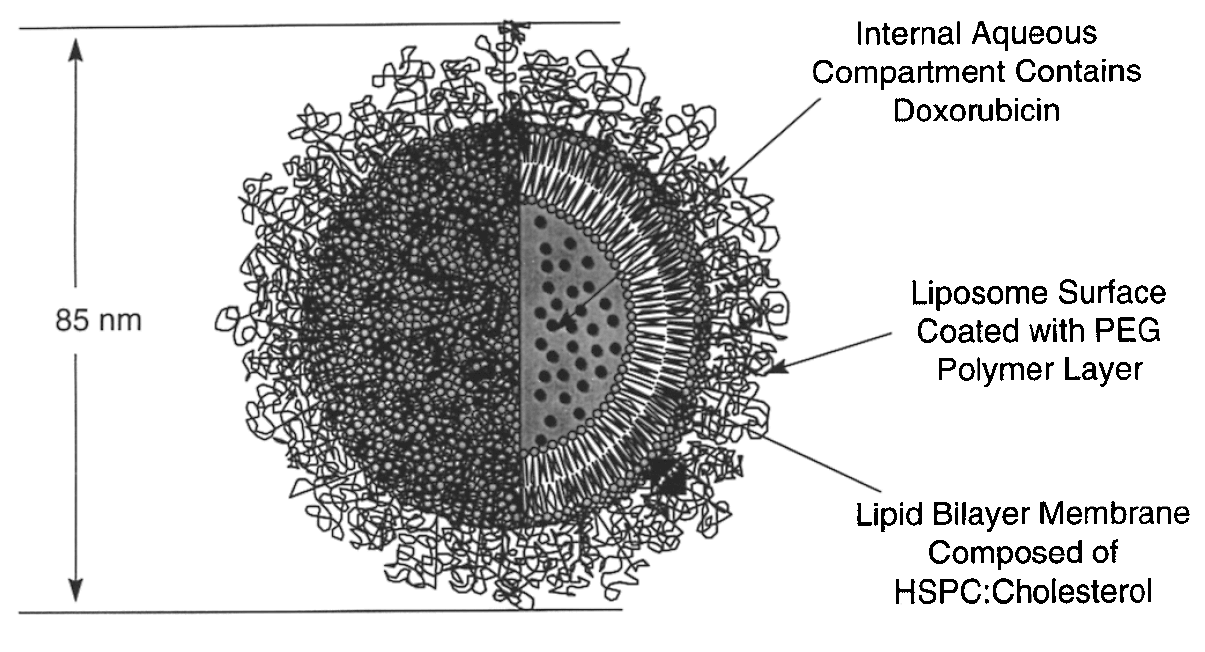
在Annamycin的结构中,通去除多柔比星蒽环4位的甲氧基,并将氨糖2ʹ位引入I基,以增加药物的亲脂性,使药物能够分布于脂质体的油相磷脂双分子层,提高脂质体的载药量。Annamycin的优化结构,还将多柔比星结构氨糖3ʹ的氨基改成羟基,氨糖3ʹ位羟基以及I基的引入,都可以减少Annamycin与Doxorubicin发生交差耐药的可能性(W Priebe., 1993)。
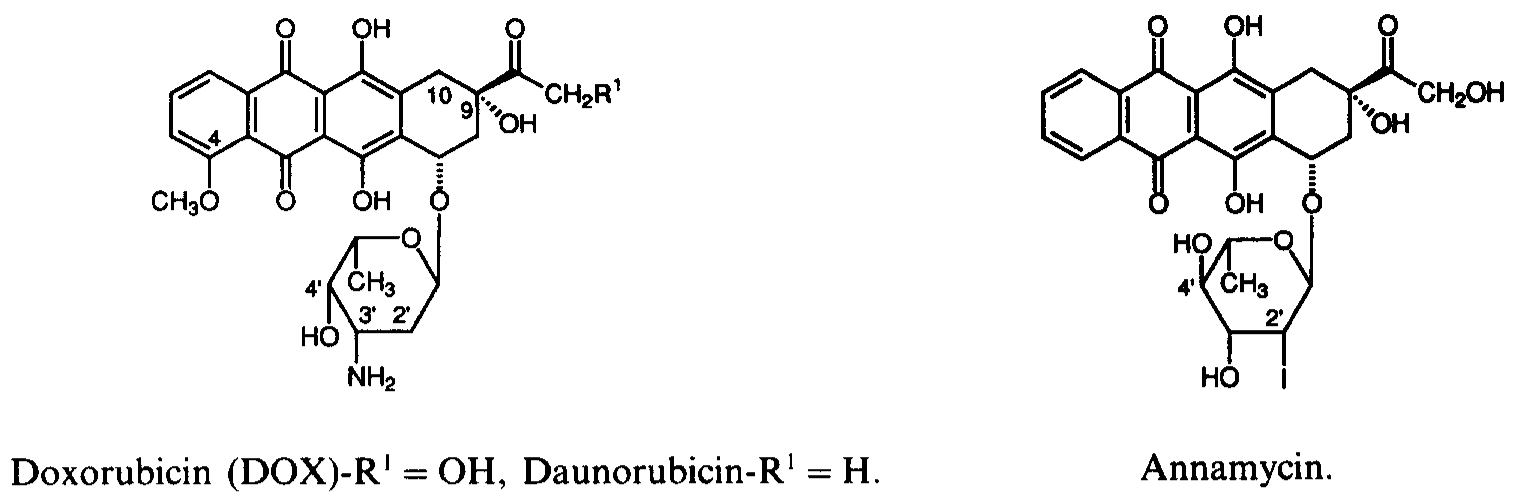
体外试验显示,对于多柔比星敏感的肿瘤细胞系,游离Annamycin和Annamycin脂质体的抗肿瘤活性与多柔比星相似,对于多药耐药肿瘤细胞系,游离Annamycin和Annamycin脂质体都展现出更强的抗肿瘤活性(Y Zou., 1994)。
Annamycin对于多柔比星敏感小鼠白血病p388细胞系的细胞毒性与多柔比星相同,但对于耐药细胞系的细胞毒性为50~100倍以上。多柔比星在敏感细胞中完全保留,在耐药细胞中快速流出。而Annamycin在敏感细胞和耐药细胞中的外排模式非常相似,表明Annamycin并不由P-糖蛋白 (Pgp,又名MDR-1)介导发生外排(Y H Ling., 1993)。
1期36例复发性实体瘤患者使用Annamycin脂质体治疗的临床试验,未发现Annamycin能够引起的心脏毒性。该试验显示Annamycin的剂量限制性毒性为血小板减少症,5例患者疑似出现过敏反应,1例患者需要停止治疗。但另人失望的是该试验未观察到肿瘤在客观指标上出现治疗反应(D J Booser., 2000)。
同样另人失望的是针对多柔比星耐药乳腺癌的2期临床试验,也未能证明Annamycin具有治疗意义(Daniel J Booser., 2002)。
2013年Meir Wetzler等人发表Annamycin纳米脂质体治疗成人复发/难治性急性淋巴细胞白血病(ALL)的1/2期临床试验结果。 8名患者完成Annamycin在最大耐受剂量 (MTD)150 mg/m2/d下使用1个治疗周期(3天)。5名患者出现完全清除外周原始淋巴细胞的迹象,其中3名患者完全清除骨髓原始细胞,3人中1名患者随后成功进行了干细胞移植,另2名患者患上肿瘤溶解综合征,在治疗反应评估之前去世(Meir Wetzler., 2013)。
2021年10月18日,Moleculin Biotech在线公布了Annamycin治疗软组织肉瘤肺转移的1B/2期临床试验中期数据。5 名患者中有 4 名表现出对治疗产生反应,其中 3 例病情延长,1例持续稳定,4例中1名患者肿瘤大小大幅减小(>30%)(Moleculin Biotech., 2021)。
2024年3月25日,Moleculin Biotech在线公布了Annamycin治疗急性髓系白血病(AML)的1B/2期临床试验中期数据。Annamycin联合阿糖胞苷(Cytarabine)做为2线治疗的完全应答率达到50%,综合完全应答率达到60%。受试验者未出现心脏毒性反应,并且毒性反应低于传统强化治疗(Moleculin Biotech., 2024)。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3