
反义寡核苷酸药物(ASO)一般含有12-28个与目标核酸碱基互补的特定序列核酸单链,可通过与目标RNA形成ASO-RNA复合双链,利用占位作用,调节目标基因的表达,也能够通过核糖核酸酶H(RNase H)清除ASO-RNA复合双链的RNA链,发挥作用。C9ORF72基因及SOD1 基因突变是家族性肌萎缩侧索硬化(ALS)前两大病因。通过ASO调节C9ORF72、SOD1等基因的功能将有助于减缓相关家庭性ALS的进展。
2023年4月25日美国FDA加速审批通过反义寡核苷酸药物Qalsody(Torfersen)用于治疗超氧化物歧化酶1(SOD1)基因突变所致肌萎缩侧索硬化(ALS)。ALS俗称“渐冻症”。Torfersen是FDA批准后第3个治疗ALS的药物,也是首款针对ALS的基因靶向疗法治疗药物。

Qalsody(Torfersen)
关于反义寡核苷酸药物概念的提出,最早可以追溯到1967年。1967年前苏联科学院西伯利亚分院的Grineva等人提出设想,使用双氯乙胺、氮芥等烷化剂对互补核苷酸片断进行修饰,来调节目标基因。1977年,Grineva等人成功将化学修饰后的互补核苷酸片断,使缬氨酸tRNA发生烷基化。同年美国国家癌症研究所(National Cancer Institute, NCI)的Paterson等人发现未经化学修饰的单链DNA,就能够使对应的RNA失去翻译功能。
1978年美国亨廷顿纪念医院(Huntington Memorial Hospital)的Zamecnik和Stephenson利用含13个碱基的脱氧核糖核酸(DNA)片断,阻止了劳氏肉瘤病毒(Rous Sarcoma Virus)在鸡胚胎中的复制和细胞转化。他们也尝试对DNA片断的3ʹ端和5ʹ端进行化学修饰来阻止核酸酶(Nuclease)对DNA片断的降解。Zamecnik和Stephenson的努力,成功实现了反义寡核苷酸(Antisense oligonucleotides,ASO)对于靶基因功能的干预,揭开了通过ASO特定序列调控目标基因的基因靶向疗法序幕。1979年,美国哈佛大学的 Donis-Keller 证实核糖核酸酶H(RNase H)能够选择性降解DNA-RNA复合双链中的RNA链,阐明了ASO清除目标RNA,调控靶基因功能的作用机制。
一般把由12-28个碱基组成的核苷酸,称为寡核苷酸(Oligonucleotide,ON)。尽管反义寡核苷酸具有无限应用前景,但在80年代,3个实现问题限制了ASO的实际应用。第一、ON结构中磷酸核糖骨架的亲水性使ASO难以进入细胞;第二、ASO合成困难,自动合成ON所需的工艺和设备尚未开发出来;第三、对于人类基因的了解还十分有限。直到1998年,美国食品药品管理局(FDA)才批准了第一个ASO类药——福米韦生(Fomivirsen)。福米韦生为特殊序列的ASO使用硫代磷酸酯取代磷酸核糖骨架中磷酸酯,即将磷酸酯上的羟基(-OH)使用巯基(-SH)进行替代。硫代磷酸酯增加了ASO的脂溶性,使ASO更容易通过细胞膜。另外脂溶性增加后,也有助于ASO在血液中与血清蛋白可逆结合,延长作用时间。尽管硫代磷酸酯改善了分布和作用时间,但也会增加潜在的炎症反应。
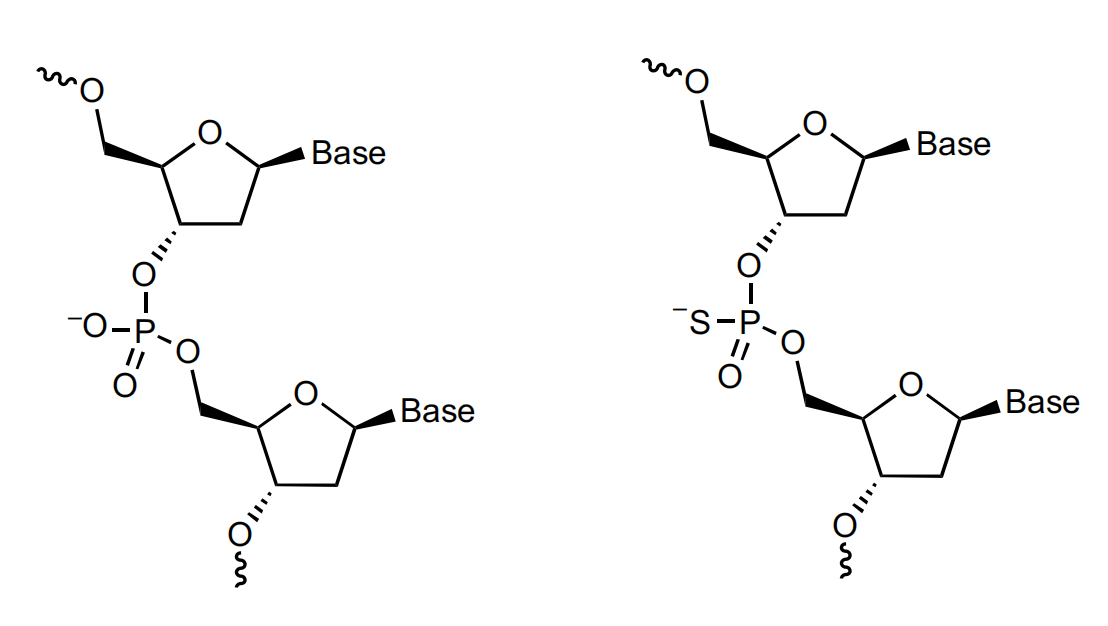
使用硫代磷酸酯结构的ASO
针对ASO磷酸核糖骨架中的核糖部分改造的策略,包括在核糖的2ʹ位引入2ʹ-MOE(2ʹ-OCH2CH2OCH3)取代基或将核糖的2ʹ位与4ʹ位进行环化。对核糖部分改造,一方面可以进一步改善ASO的亲脂性;另一方面可以使ASO耐受核酸酶的降解,并减少硫代磷酸酯引起的潜在炎症反应。尽管核糖2ʹ端的改造会影响RNase H降解ASO-RNA复合双链中的RNA链,但核糖2ʹ位改造的ASO依旧可以通过占位,调节目标基因发挥作用。由于RNase H需要至少5个连续的碱基序列,8-10个连续碱基序列可达到最佳活性,如需保留核糖2ʹ位改造的ASO对目标RNA的降解作用,可以通过混合排列的方式设计ASO,如使用8个连续不改变核糖2ʹ位的核酸片断作为中心区,两端分别引入多个使用核糖2ʹ位改造后的碱基序列。混排后,一方面进一步改善了ASO在体内的分布,减少硫代磷酸酯潜在的炎症反应,并可使ASO耐受核酸酶;另一方面,ASO-RNA复合双链中的RNA可以被RNase H降解,RNA降解后的ASO可以继续用于降解其它目标RNA。
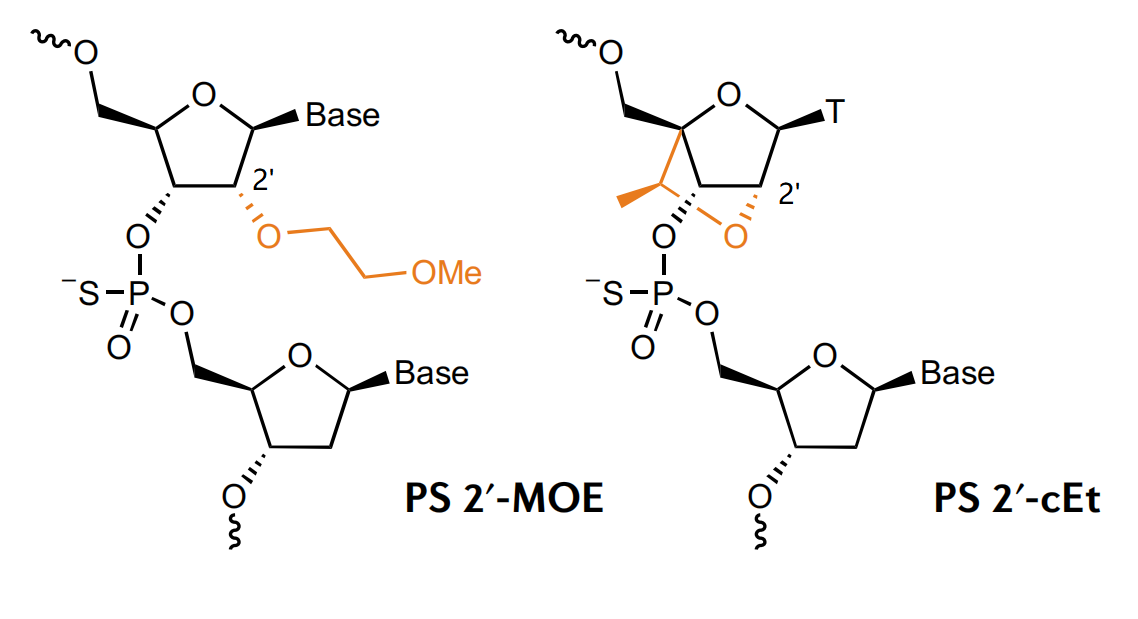
使用硫代磷酸酯结构并对核糖2ʹ位改造的ASO
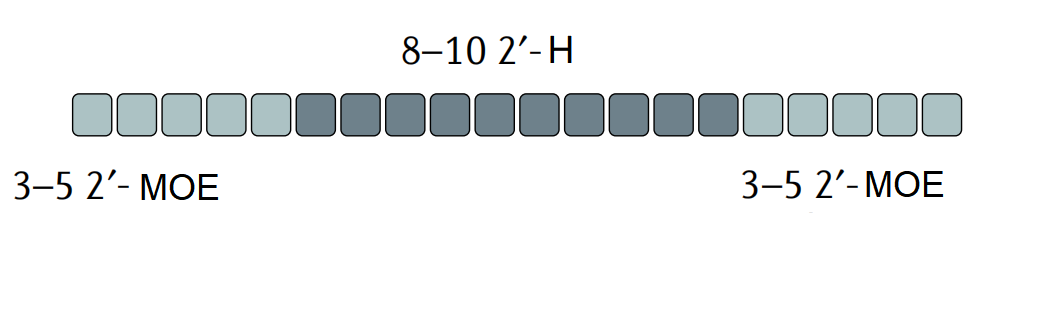
混合排列方式设计的ASO
C9ORF72基因突变是引起家族性ALS的第一大常见原因,约占家族性ALS的25-40%的病例,全部ALS病例的6%。C9ORF72基因突变还会导致另一种神经退行性疾病,额颞叶痴呆(FTD)。约占FTD的25%。患者可能同时发生ALS和FTD,也有部分患者仅表现为ALS或FTD。关于C9ORF72基因突变后的对神经功能影响的机制,尚不完全清楚。
SOD1基因突变是引起家族性ALS的第二大常见原因,约占家族性ALS的10-20%的病例,全部ALS病例的1-2%,目前已发现150多种SOD1基因突变。正常的SOD1有助于分解细胞内的毒性产物,从而避免破坏细胞。运动神经元和星形胶质细胞的SOD1突变基因,会形成在结构上出现错误的折叠SOD1蛋白,这类蛋白质可发生聚集。聚集物会进一步影响正常的细胞功能,并可能导致细胞内的其他蛋白质也发生错误折叠和聚集。
尽管3期临床研究未能证明在Torfersen 在改善《ALS功能评分量表(ALSFRS-R)》评分方面优于安慰剂对照组。但基于Torfersen组脑脊液中SOD1蛋白和血液中神经损伤标志物神经丝蛋白轻链(NfL)下降水平显著优于安慰剂对照组,2023年4月25日美国FDA加速审批通过Biogen渤健的Qalsody(Torfersen)用于治疗SOD1基因突变所引起的家族性ALS。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3