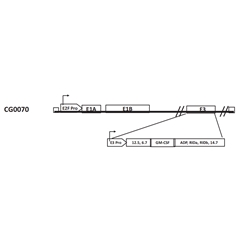
Cretostimogene Grenadenorepvec是由CG Oncology开发的重组条件复制溶瘤5型腺病毒(Ad5)。通过在病毒基因碱基中插入E2F-1启动子和SV40晚期polyA化信号实现溶瘤病毒特异性在肿瘤内部表达复制,并通过加入人粒细胞-巨噬细胞集落刺激因子(GM-CSF)cDNA序列表达GM-CSF来增强持久的抗肿瘤免疫作用。
结构:
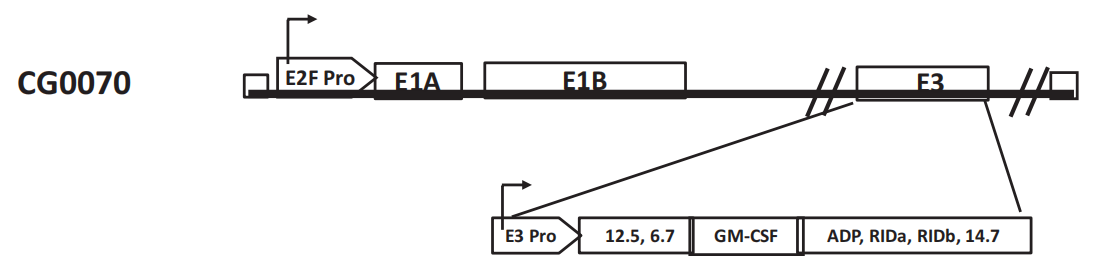
介绍:
Cretostimogene Grenadenorepvec(开发编号CG0070)是由CG Oncology开发的重组条件复制溶瘤5型腺病毒(Ad5)。
CG0070最初由Cell Genesys开发。2009年Cell Genesys与BioSante合并。2010年 Cold Genesy从BioSante购得CG0070的开发权利。2020年Cold Genesy更名为CG Oncology。
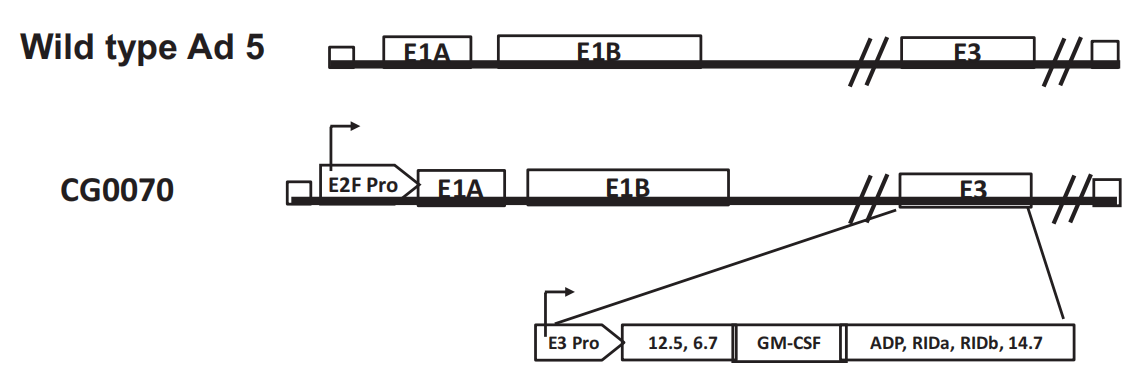
CG0070(Ad5-E2F-E1A-E3-GMCSF)的碱基序列加入人E2F-1启动子以替代通过内源性E1A启动子启动翻译,并在E2F-1启动子的上游插入猴病毒40(SV40)晚期多聚腺苷(polyA)化信号,CG0070还使用人粒细胞-巨噬细胞集落刺激因子(GM-CSF)cDNA序列取代E3 19 kDa糖蛋白(gp19kD)编码区。
E2F-1细胞转录因子是周期激活蛋白,能够促进细胞周期的进行,受转录辅助抑制物视网膜母细胞瘤抑制蛋白(Rb)调控。Rb能够抑制E2F-1的活化,阻止细胞周期的进行。膀胱、头颈部、结肠、前列腺、黑色素瘤等肿瘤存在Rb的表达缺陷。导致E2F-1过度活化。因此溶瘤病毒碱基序列插入E2F-1启动子,有助于实现溶瘤病毒在肿瘤细胞内特异性复制转录,并产生细胞毒性。插入SV40晚期polyA化信号,可以强化在E2F-1启动子启动翻译,提高溶瘤病毒对于肿瘤细胞的选择性。溶瘤病毒表达GM-CSF,有助于获得持久的抗肿瘤免疫作用。此外,CG0070采用膀胱内给药,增加对于膀胱癌的靶向性。
2012年James M Burke等人发表CG0070的1期临床研究结果。35名非肌层浸润性膀胱癌患者接受不同剂量(1×1012、3×1012、 1×1013、3×1013 Vp)CG0070膀胱内给药,平均完全缓解率达到 48.6%,中位数完全缓解持续时间达到10.4个月(James M Burke., 2012)。
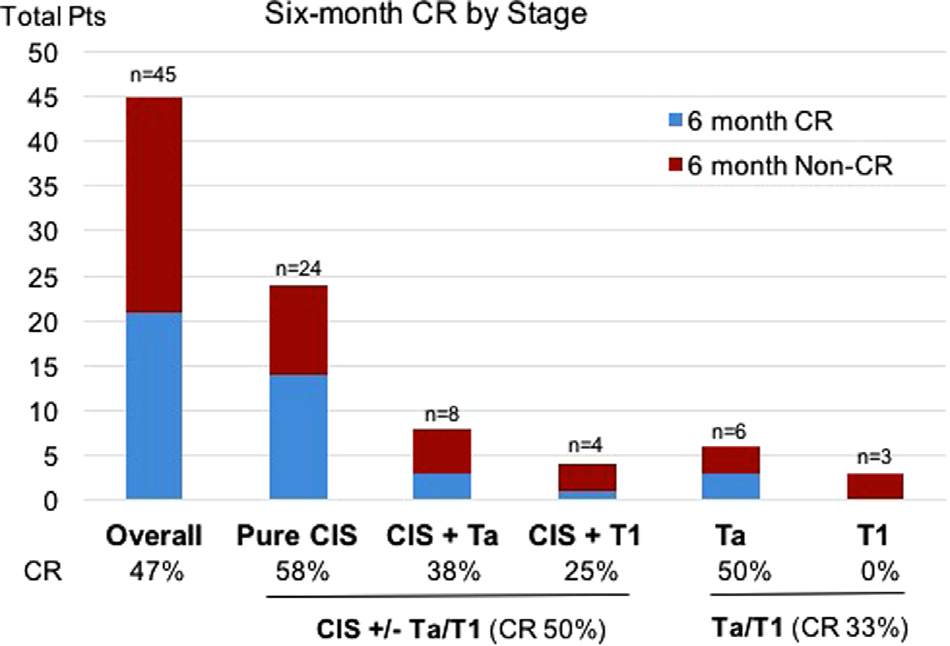
2018年Vignesh T Packiam人发表CG0070的2期临床中期研究结果。45名卡介苗(BCG)无反应的高级别非肌肉浸润性膀胱癌患者,每周1次,连续6周CG0070(1×10^12Vp)膀胱内给药,随访6个月的完全缓解率达到47%(Vignesh T Packiam., 2018)。
2023年11月23日CG Oncology在线公布了Cretostimogene Grenadenorepvec(CG0070)治疗高风险非肌肉浸润性膀胱癌3期临床试验(BOND-003)中期研究结果。以2023年10月5日为截点,66名患者至少随访3个月,任何时候的完全缓解率达到75.7%(CG Oncology., 2023)。
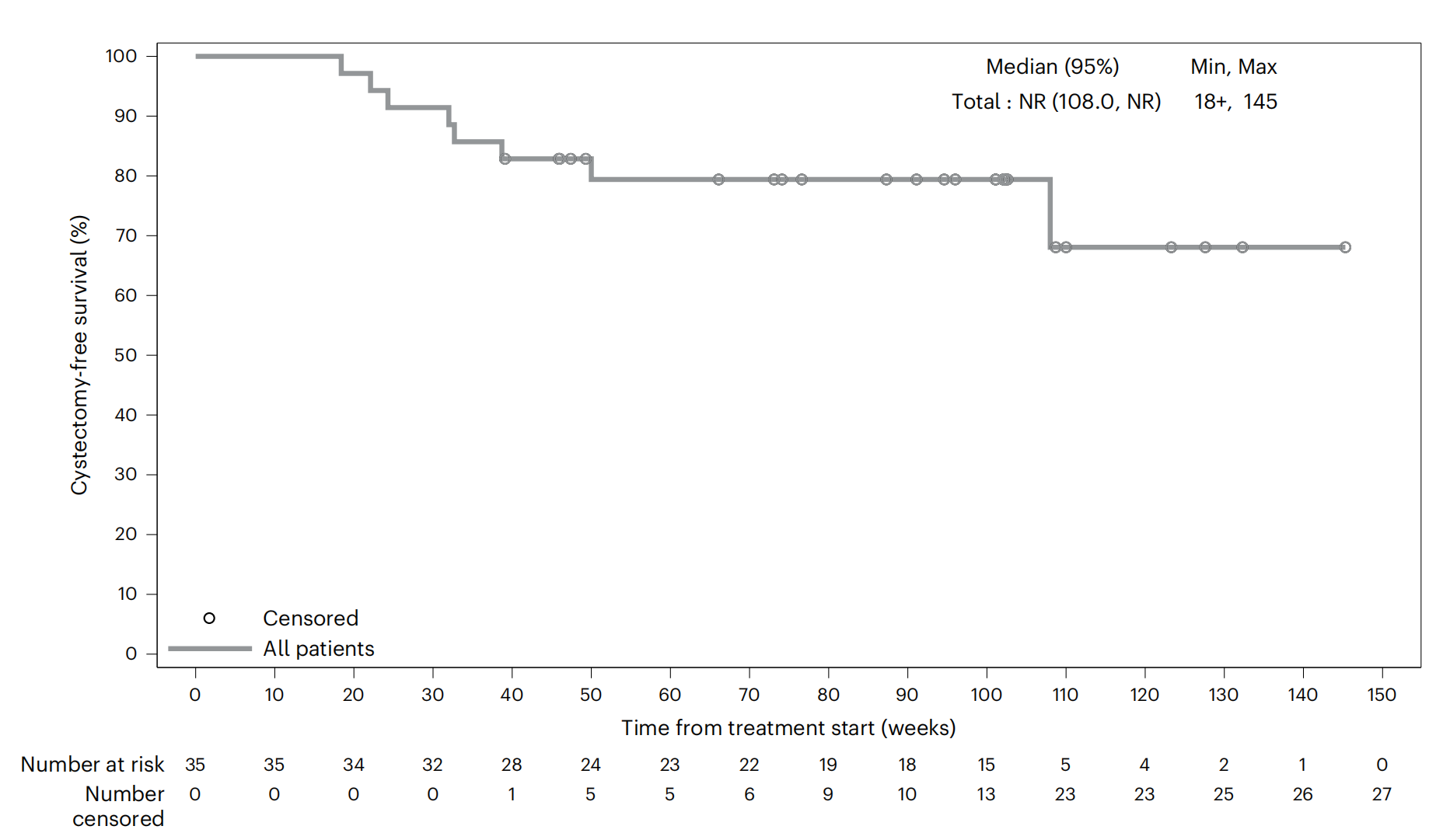
2024年,Roger Li等人发表Cretostimogene Grenadenorepvec联合帕博利珠单抗治疗卡介苗 (BCG) 治疗无反应原位非肌肉浸润性膀胱癌(CIS)2期临床试验CORE-001的试验结果。该试验共纳入35名受试者,使用Cretostimogene联合帕博利珠单抗治疗。受试者在接受经尿道膀胱肿瘤电切术(TURBT)后,使用Cretostimogene每周1次,诱导治疗6周,然后在第 3、6、9、12 和 18 个月使用Cretostimogene Grenadenorepvec持续治疗3周(1次/周)。如在3个月的评估中,持续存在CIS,或存在高级别Ta期膀胱癌,受试者重新进入诱导期。帕博利珠单抗从治疗开始使用24个月。至第12个月受试者的完全缓解率为57.1%(95% CI 40.7-73.5%)。第3个月完全缓解率为82.9%。中位数随访时间为26.5个月,尚未达到中位缓解持续时间(95% CI 15.7-未达到)。第24个月的完全缓解率为51.4%(95%CI 34.9-68.0%)。没有患者进展到肌层浸润性膀胱癌。Cretostimogene不良事件为低级别、自限性、主要局限于膀胱相关症状,免疫相关不良反应仅与帕博利珠单抗有关,35 例受试者有5 例(14.3%) 出现 3 级治疗相关性不良反应,均与帕博利珠单抗有关,没有证据表明Cretostimogene与帕博利珠单抗存在叠加或协同毒性(Roger Li., 2024)。
(校对20240612)

免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
关注“药研苑”公众号,及时掌握最新的药物研发动态。
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


溶瘤病毒483
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3