
Icotrokinra 是大环肽IL-23受体拮抗剂。尽管口服生物利用度低,由于Lcotrokinra与IL-23受体细胞外结构域具有高亲和力,可以通过口服实现全身给药。
结构:
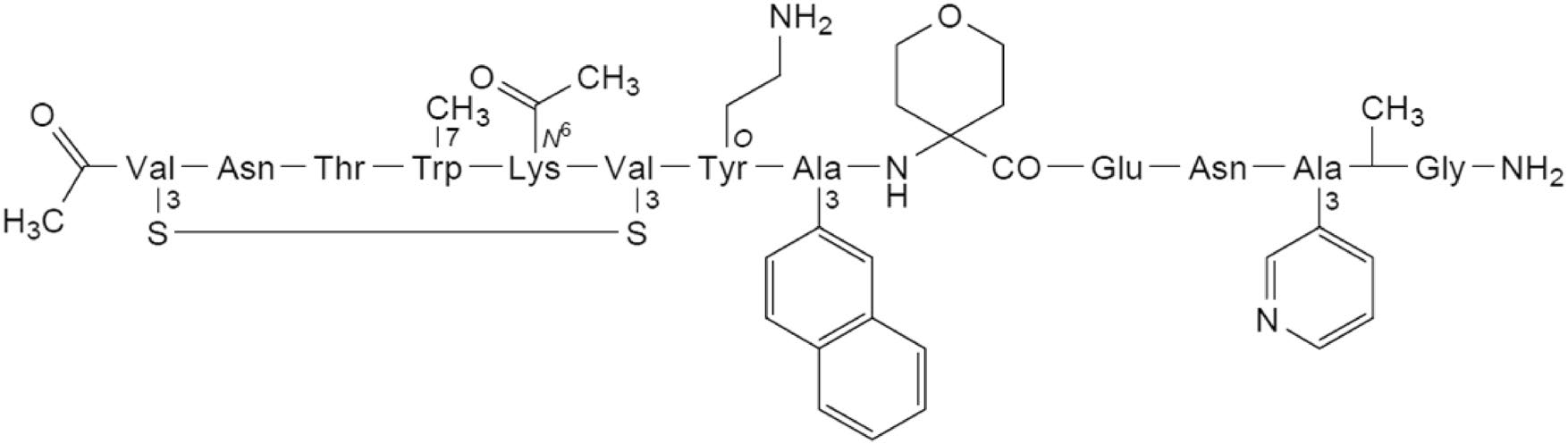
介绍:
Icotrokinra 是强生Johnson & Johnson(研发代号JNJ-77242113,JNJ-2113)与Protagonist Therapeutics(研发代号PN-235)合作开发的大环肽(Macrocyclic Peptide)口服IL-23受体(IL-23R)拮抗剂。
Icotrokinra 与作用于IL-23受体细胞外结构域(ECD),阻断IL-23对于IL-23R的激动作用。对大鼠火炎症性肠病研究显示,尽管Lcotrokinra的口服生物利用度低,但可检测到血浆浓度。由于Icotrokinra 与IL-23R ECD具有高亲和力(KD=7.1 pM),大鼠药代动力学-药效学模型研究显示,Icotrokinra 可以通过口服实现全身给药(Anne M Fourie., 2024)。
2024年,Laura K Ferris等人发表Icotrokinra 用于斑块状银屑病2b期临床试验FRONTIER-2长期扩展耐研究结果。FRONTIER-2为2b临床试验,在16周治疗后,进入长期扩展阶段。至第52周,Lcotrokinra 100mg bid组治疗反应率最高,76% 达到《银屑病面积和严重程度指数评分》改善≥75%(PASI 75)。 64%的患者达到PASI 90。74%达到《研究者整体评估量表(IGA)》评分为0-1分(皮肤光洁或几乎光洁)。40% 的患者达到PASI 100。43%的患者达到IGA 0分。从第16周至第 56 周,59%的JNJ-77242113使用患出现 ≥1 次不良事件 (AE)。严重AE发生率为 4%,研究人员认为与治疗无关(Laura K Ferris., 2024)。
2024年11月18日,强生宣布Icotrokinra 用于12岁及以上青少年成人和中重度斑块状银屑病(PsO)3期临床试验ICONIC-LEAD达到主要复合终点。至第16周,Icotrokinra组近三分之二(64.7%)的患者达到《研究者整体评估量表(IGA)》评分为0-1分(皮肤光洁或几乎光洁),49.6%的患者达到《银屑病面积和严重程度指数评分》改善≥90%(PASI 90)。而安慰剂组分别为8.3%和4.4%。治疗期不良事件(TEAE)的发生率Icotrokinra组和安慰剂组相似,分别有49.3%和49.1%的患者发生不良事件(AE)(Johnson., 2024)。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3