来源:诺华 796
2025年11月5日, 诺华Novartis宣布其放射配体疗法(RLT)药物镥[177Lu]特昔维匹肽注射液(派威妥®)获得国家药品监督管理局批准,用于治疗既往接受过雄激素受体通路抑制剂(ARPI)后疾病进展且适合延迟化疗的成人前列腺特异性膜抗原(PSMA)阳性转移性去势抵抗性前列腺癌(mCRPC),以及既往接受过ARPI和紫杉类化疗后疾病进展的成人PSMA阳性转移性去势抵抗性前列腺癌。

此次镥[177Lu]特昔维匹肽获批,基于全球3期临床试验VISION和PSMAfore研究,以及对于中国桥接研究的试验结果。
VISION为国际多中心、随机、开放标签3期临床试验,共纳入831 例PSMA阳性转移性去势抵抗性前列腺,以及既往使用紫杉类和雄激素受体通路抑制剂后出现进展的患者。入组患者按2:1比例随机接受镥[177Lu]特昔维匹肽(每6周静脉输注7.4 GBq±10%,最多6个周期)联合研究者选择的最佳标准治疗(bSOC),或仅接受bSOC治疗。研究结果显示,镥[177Lu]特昔维匹肽联合组和bSOC组影像学无进展生存期(rPFS)分别为8.7和3.4 个月,镥[177Lu]特昔维匹肽组影像学无进展或死亡风险降低60%(HR 0.40,P<0.001)。镥[177Lu]特昔维匹肽联合组和bSOC组总生存期(OS)分别为15.3 和11.3 个月,镥[177Lu]特昔维匹肽组死亡风险降低38%(HR 0.62, P<0.001)。在患者的生活质量和功能评分(FACT-P )恶化时间方面,镥[177Lu]特昔维匹肽联合组降低54%的恶化风险(9.7 个月vs. 2.4 个月,HR 0.46)。在简明疼痛量表-简表(BPI-SF)疼痛强度恶化时间方面,镥[177Lu]特昔维匹肽联合组降低56%的恶化风险(9.7 个月vs. 2.4 个月,HR 0.46)。对于基线时至少有一个可测量靶病灶的患者,镥[177Lu]特昔维匹肽联合组和 bSOC组的完全缓解率(CR)分别为9.2%和0,基线有可测量病灶患者的客观缓解率(ORR)分别为51%和3%。PSA(前列腺特异抗原)水平相比基线值下降≥50%(PSA50)的比例分别为46%和7.1%。在安全性方面,≥3级的血液学不良事件包括血红蛋白降低,镥[177Lu]特昔维匹肽联合组和 bSOC组分别为15%(80/ 529)和6%(13 / 205);淋巴细胞浓度下降分别为51%(269)和19%(39)和血小板计数下降分别为9%(49)和2%(5)。镥[177Lu]特昔维匹肽联合组发生5例(1%)治疗相关性死亡病例,包括全血细胞减少(2)、骨髓衰竭(1)、硬膜下血肿(1)和颅内出血(1)(Karim Fizazi., 2023)。
PSMAforeu为国际多中心、前瞻性、随机、开放标签3期临床试验。共纳入468例既往经一种雄激素受体通路抑制剂(ARPI)治疗、未接受化疗治疗的转移性去势抵抗性前列腺癌(mCRPC)患者。入组患者按1:1的比例随机接受镥[177Lu]特昔维匹肽注射液(每六周静脉输注7.4 GBq,最多6个周期)或换用另一种ARPI(阿比特龙或恩扎卢胺)。研究结果显示,镥[177Lu]特昔维匹肽组与换用另一种ARPI组相比,提高了影像学无进展生存期(rPFS 11.60个月vs.5.59个月,HR 0.49, P<0.001)、基线有可测量病灶的客观缓解率(ORR)50% vs. 15%)、完全缓解(CR)率(21% vs.4%)、达到PSA50的比例(51% vs. 17%)、FACT-P恶化时间(9.17个月 vs. 4.60个月,HR 0.49)、BPI-SF疼痛强度恶化时间(8.15个月 vs. 4.50个月,HR 0.65)、至PSA进展的中位时间(10.64个月 vs. 4.24个月,HR 0.40)、以及基线有可测量病灶的患者的影像学软组织病灶缓解持续时间(NE vs. 10.05个月)。在安全性方面,镥[177Lu]特昔维匹肽组≥3级不良事件的发生率低于换用另一种ARPI组(35.2% vs. 49.1%)。最常见的≥3级不良事件为贫血,镥[177Lu]特昔维匹肽组和换用另一种ARPI组分别为6%(14)和7%(16)。镥[177Lu]特昔维匹肽组未发生治疗相关性死亡病例,换用另一种ARPI组发生1例(脑血管意外)(Karim Fizazi., 2025)
镥[177Lu]特昔维匹肽(lutetium lu 177 vipivotide tetraxetan,[177Lu]Lu-PSMA-617)属于放射配体疗法(RLT),利用螯合携带放射性核素镥[177Lu],由链接子(Linker)与含C端谷氨酸残基肽的PSMA特异性配体相结合。镥[177Lu]的半衰期为6.647天,利于生产和运输,组织穿透力<3 mm。对病灶外影响小。PSMA(前列腺特异性膜抗原)又称谷氨酸羧肽酶Ⅱ,能够特异性切割肽链C端的谷氨酸残基。镥[177Lu]特昔维匹肽中配体结构,利用PSMA对底物的高特异性,发挥靶向作用。镥[177Lu]特昔维匹肽的中的链接子除了能够避难螯合镥[177Lu]对配体的负面影响之外,还用于改善药物代谢动力学。
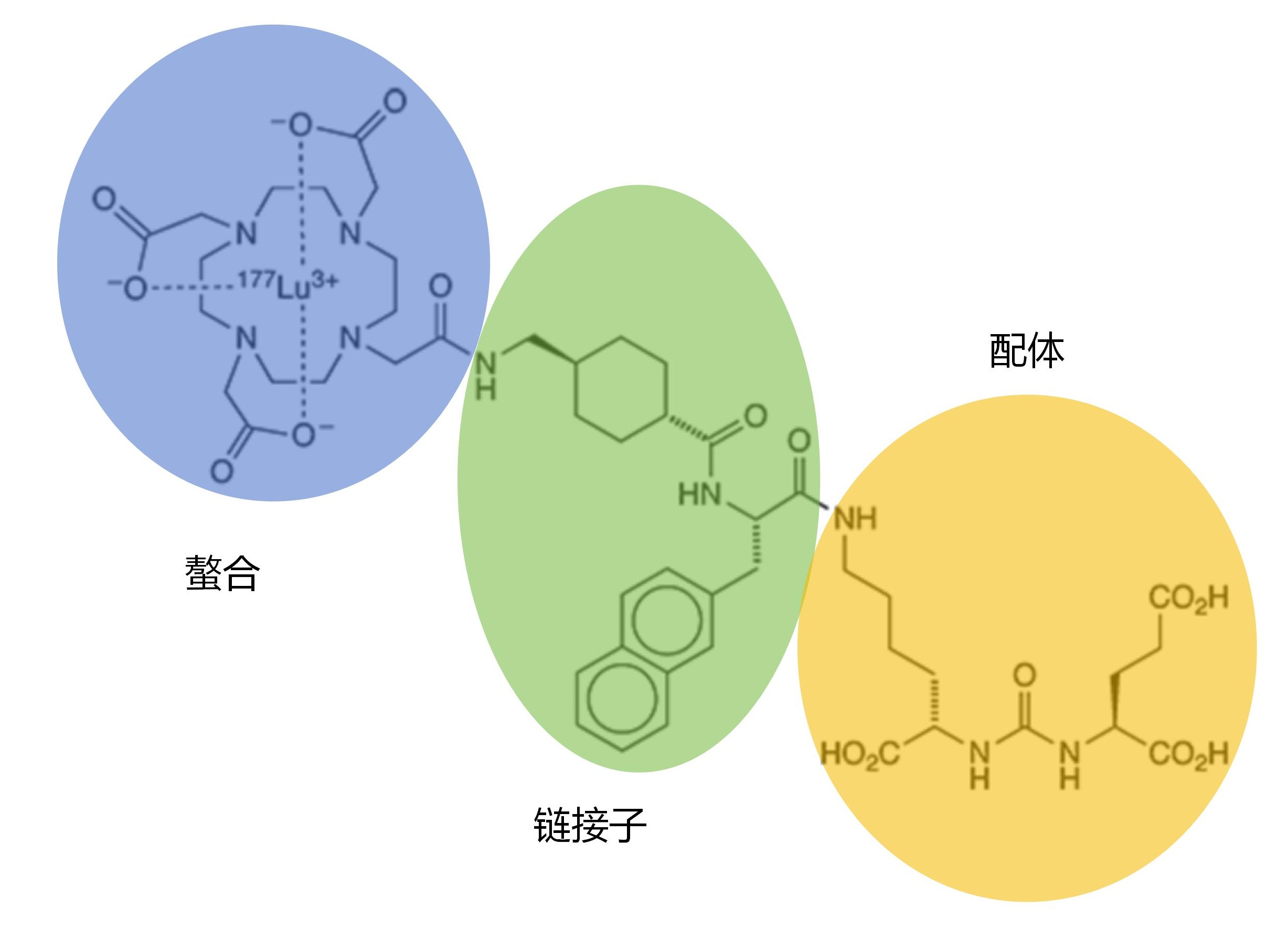
镥[177Lu]特昔维匹肽
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2024年10月24日,上海海和药物研究开发股份有限公司和三生制药共同宣布:三生制药子公司沈阳三生制药有限责任公司获得海和药物子公司诺迈西(上海)医药科技有限公司(旗下产品紫杉醇口服溶液在中…
发布日期:2024-10-24 浏览数:1488

2024年10月8日,亚盛医药宣布APG-2449已获国家药品监督管理局(NMPA)药物审评中心(CDE)临床试验许可,将开展针对二代间变性淋巴瘤激酶(ALK)TKI耐药或不耐受的非小细胞肺癌(NSCLC)患者,以…
发布日期:2024-10-08 浏览数:1359

2024年11月2日,深圳微芯生物科技股份有限公司宣布收到国家药监局核准签发的,关于西奥罗尼联合PD-(L)1单抗及化疗一线治疗广泛期小细胞肺癌3期临床试验申请的《药物临床试验批准通知书》。
发布日期:2024-11-02 浏览数:1178

2024年7月28日,科兴制药宣布注射用紫杉醇(白蛋白结合型)(Apexelsin®,简称白蛋白紫杉醇)获得欧盟批准。
发布日期:2024-07-28 浏览数:1145
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3