
伊布替尼(Ibrutinib,研发编号PCI-32765)是第一个上市的BTK抑制剂,能够与BTK ATP结合域的Cys-481形成不可逆共价键使布鲁顿酪氨酸激酶(BTK)失活,阻断B细胞受体(BCR)信号通路,抑制B细胞瘤的增殖。
结构:
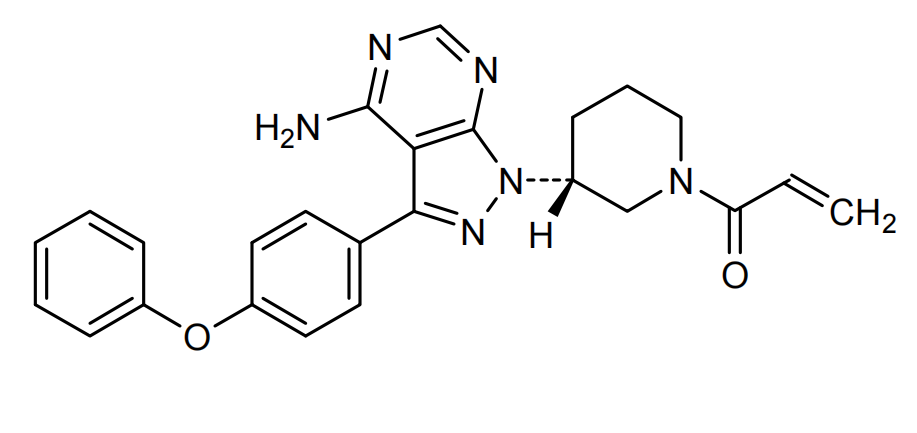
介绍:
伊布替尼(Ibrutinib,研发编号PCI-32765)是第一个上市的BTK抑制剂,由Celera Genomics开发,能够与BTK ATP结合域的Cys-481形成不可逆共价键使布鲁顿酪氨酸激酶(BTK)失活,阻断B细胞受体(BCR)信号通路,抑制B细胞瘤的增殖。
2007年Celera Genomics的hengying Pan等人报道报道含4-氨基-3-(4-苯氧基苯基)-1H-吡唑并[3,4-d]嘧啶结构的化合物,具有抑制BTK的作用,能够与BTK ATP结合域的Cys-481形成不可逆的共价键使BTK失活。在该化合物的基础上通过替代吡唑环上的取代基得到作用更强的伊布替尼(Zhengying Pan., 2007)。
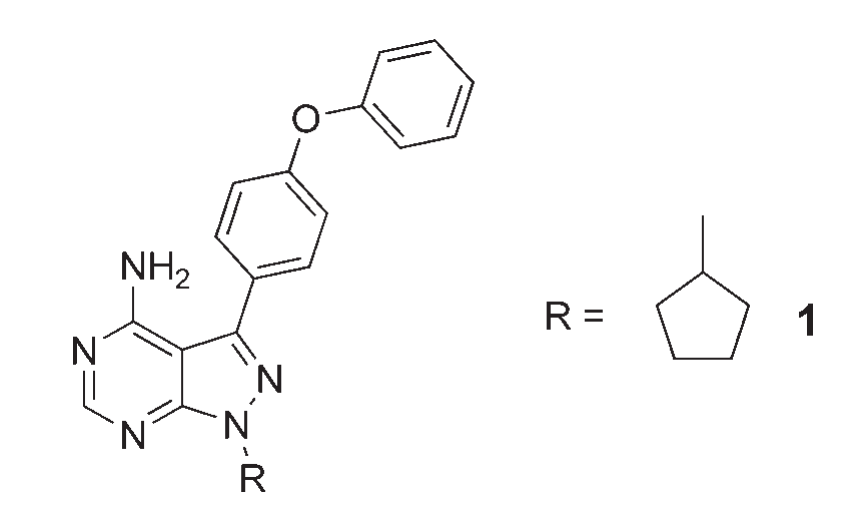
2006年Pharmacyclics从Celera Genomics购得伊布替尼的开发权利。2011年强生(Johnson & Johnson)的子公司Janssen Biotech与Pharmacyclics签订协议与Pharmacyclics共同开发伊布替尼(Johnson & Johnson., 2011)。
2013年7月4日期《The New England journal of medicine》发表伊布替尼治疗复发性慢性淋巴细胞白血病(CLL)1b-2期试验结果。 2个剂量组,420 mg/天(51名)和840 mg/天(34名)患者的总体反应率均达到71%,部分反应率分别为20%和15%(John C Byrd., 2013)。
2013年8月8日期《The New England journal of medicine》发表伊布替尼治疗复发或难治性套细胞淋巴瘤(MCL)2期试验结果。 111名患者,治疗剂量为560 mg/天,患者,总体反应率均为21%,部分反应率分别达到47%(Michael L Wang., 2013)。
2013年11月13日,FDA基于上述研究结果批准伊布替尼(商品名Imbruvica)用于治疗套细胞淋巴瘤,成为FDA第3个治疗套细胞淋巴瘤的药物。
2014年2月12日,FDA批准伊布替尼用于既往至少接受过一种治疗的慢性淋巴细胞白血病。2014 年7月28日,FDA批准伊布替尼用于染色体7p缺失慢性淋巴细胞性白血病。2015 年1月2日,FDA批准伊布替尼用于华氏巨球蛋白血症。
2015年12月17日期《The New England journal of medicine》发表伊布替尼治疗慢性淋巴细胞白血病(CLL)3期试验RESONATE-2的结果。 共269名患者,接受420 mg/天伊布替尼或苯丁酸氮芥进行治疗。伊布替尼组的进展或死亡风险比苯丁酸氮芥低84%(P<0.001),伊布替尼组的总体反应率均显著高于苯丁酸氮芥(86% vs. 35%, P<0.001).在安全性方面,伊布替尼组使血红蛋白和血小板水平较基线值持续升高的比率更高。在接受伊布替尼治疗的患者中,至少有20%发生的任何级别的不良事件,包括腹泻、疲劳、咳嗽和恶心;在伊布替尼组中,有4例患者出现3级出血,1例出现4级出血。伊布替尼组中共有87%的患者继续服用伊布替尼。(Jan A Burger., 2015)。2016年3月4日,FDA基于上述研究结果批准伊布替尼用于慢性淋巴细胞白血病的一线治疗。
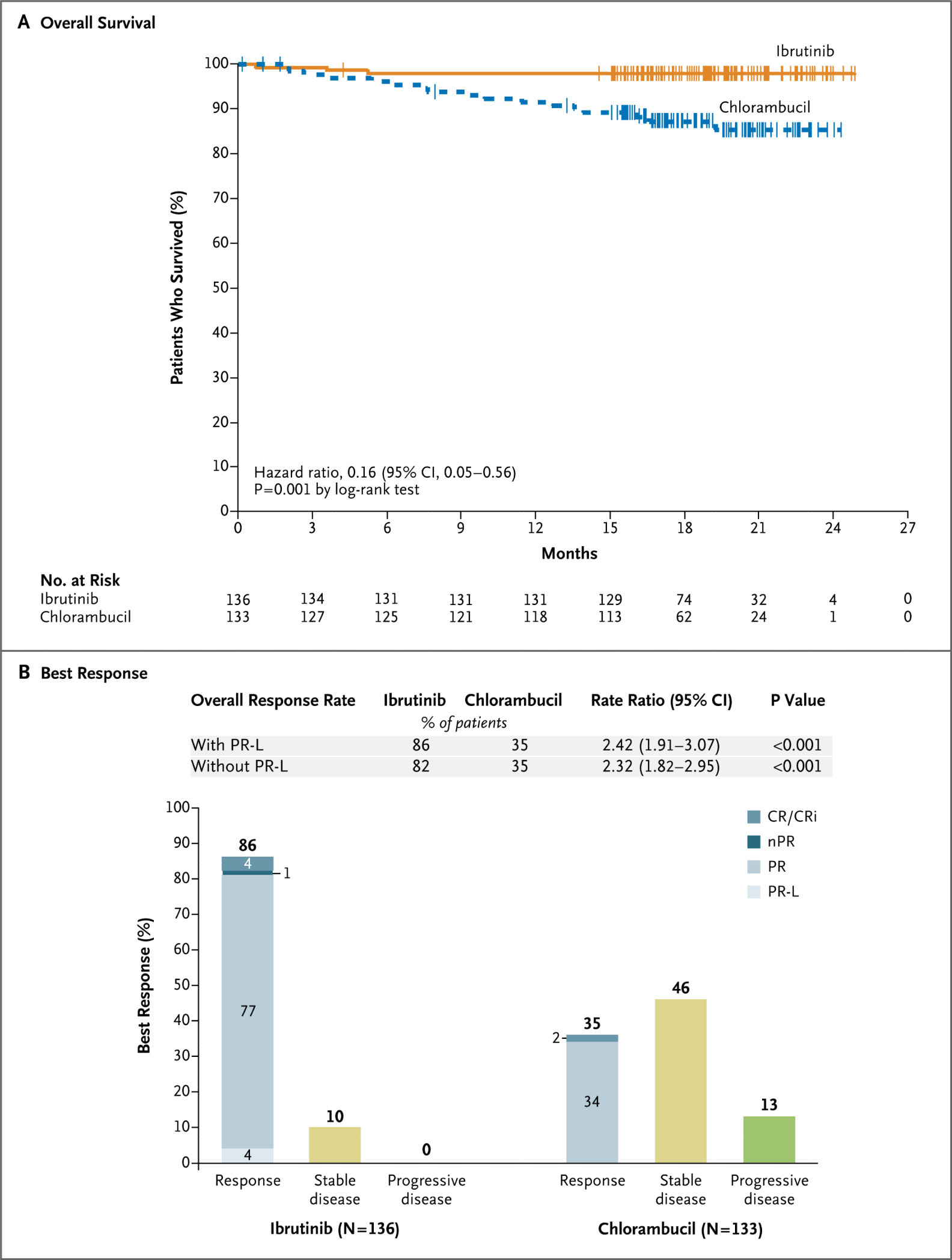
2016年2月期《The Lancet. Oncology》发表伊布替尼治疗复发可难性性慢性淋巴细胞白血病(CLL)或小淋巴细胞瘤3期试验HELIOS的结果。共578名患者,随机接受420 mg/天伊布替尼联合苯达莫司汀及利妥昔单抗或安慰剂联合苯达莫司汀及利妥昔单抗进行治疗。伊布替尼组的进展或死亡风险比安慰剂组84%(P<0.001),伊布替尼组的总体反应率均显著高于安慰剂组(86% vs. 35%, P<0.001)伊布替尼组18个月无进展生存率为79%,安慰剂组为24%(p<0.0001)(Asher Chanan-Khan., 2016)。2016年5月9日,FDA基于上述研究结果批准伊布替尼用于小淋巴细胞瘤。
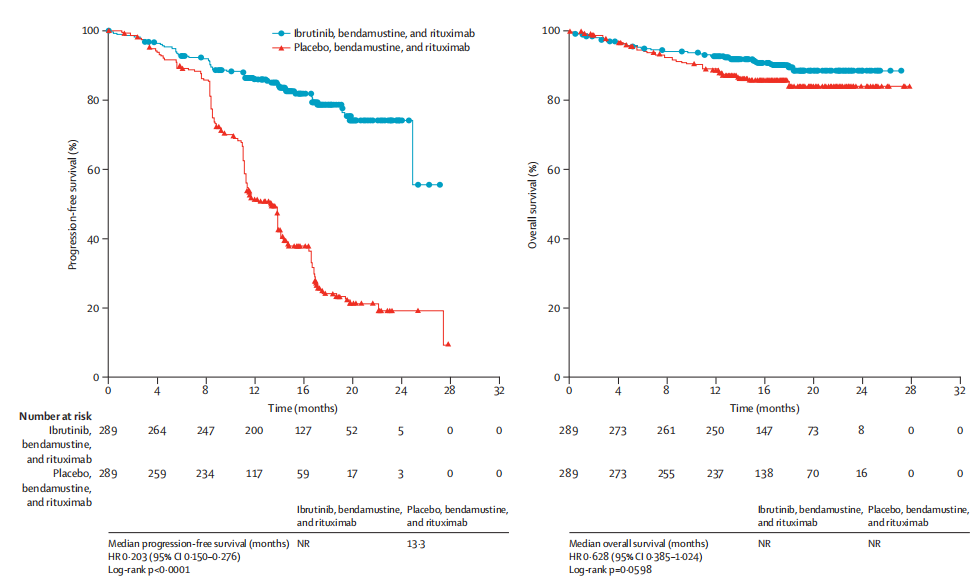
2017年1月19日FDA批准伊布替尼用于复发及难治性边缘区淋巴瘤。2017年8月2日FDA批准伊布替尼用于慢性移植物抗宿主病。 2018年8月27日FDA批准伊布替尼联合利妥昔单抗用于华氏巨球蛋白血症。 2019年1月29日FDA批准伊布替尼联合奥妥珠单抗用于慢性淋巴细胞白血病。2019年1月29日FDA批准伊布替尼联合奥妥珠单抗用于慢性淋巴细胞白血病。 2020年4月21日FDA批准伊布替尼联合利妥昔单抗用于慢性淋巴细胞白血病。2022年7月24日FDA批准伊布替尼用于儿童慢性移植物抗宿主病。2023年 4月6日日FDA批准伊布替尼用于既往至少接受过一种治疗的套细胞淋巴瘤及或既往至少接受过一种CD20为基础的边缘区淋巴瘤。2024年 2月26日日FDA批准伊布替尼口服混悬剂用于成人慢性淋巴细胞白血病/小淋巴细胞瘤、华氏巨球蛋白血症、及既往至少接受过一种全身治疗失败的慢性移植物抗宿主病。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3