
Resmetirom(研发编号MGL-3196,商品名Rezdiffra)是Madrigal Pharmaceuticals开发的甲状腺激素受体β(THRβ激动剂),能够调控肝内脂质代谢,逆转肝脏脂肪沉积。与甲状腺激素T3相比,由于与THRα亲和性较弱,避免了激动心血管THRα引起的不良反应。
结构:
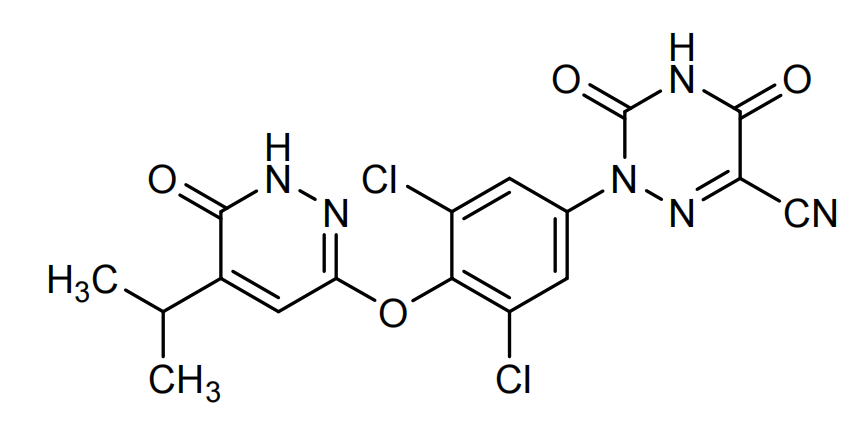
介绍:
Resmetirom(研发编号MGL-3196,商品名Rezdiffra)是Madrigal Pharmaceuticals开发的甲状腺激素受体β(THRβ激动剂),口服,一天一次。
THRβ激动剂能够调控肝内脂质代谢,逆转肝脏脂肪沉积。与甲状腺激素T3(三碘甲状腺原氨酸)相比,选择性THRβ激动剂,由于与甲状腺激素受体α(THRα)不具有亲和性或亲和性较弱,避免或有减少激动心血管THRα引起的不良反应。
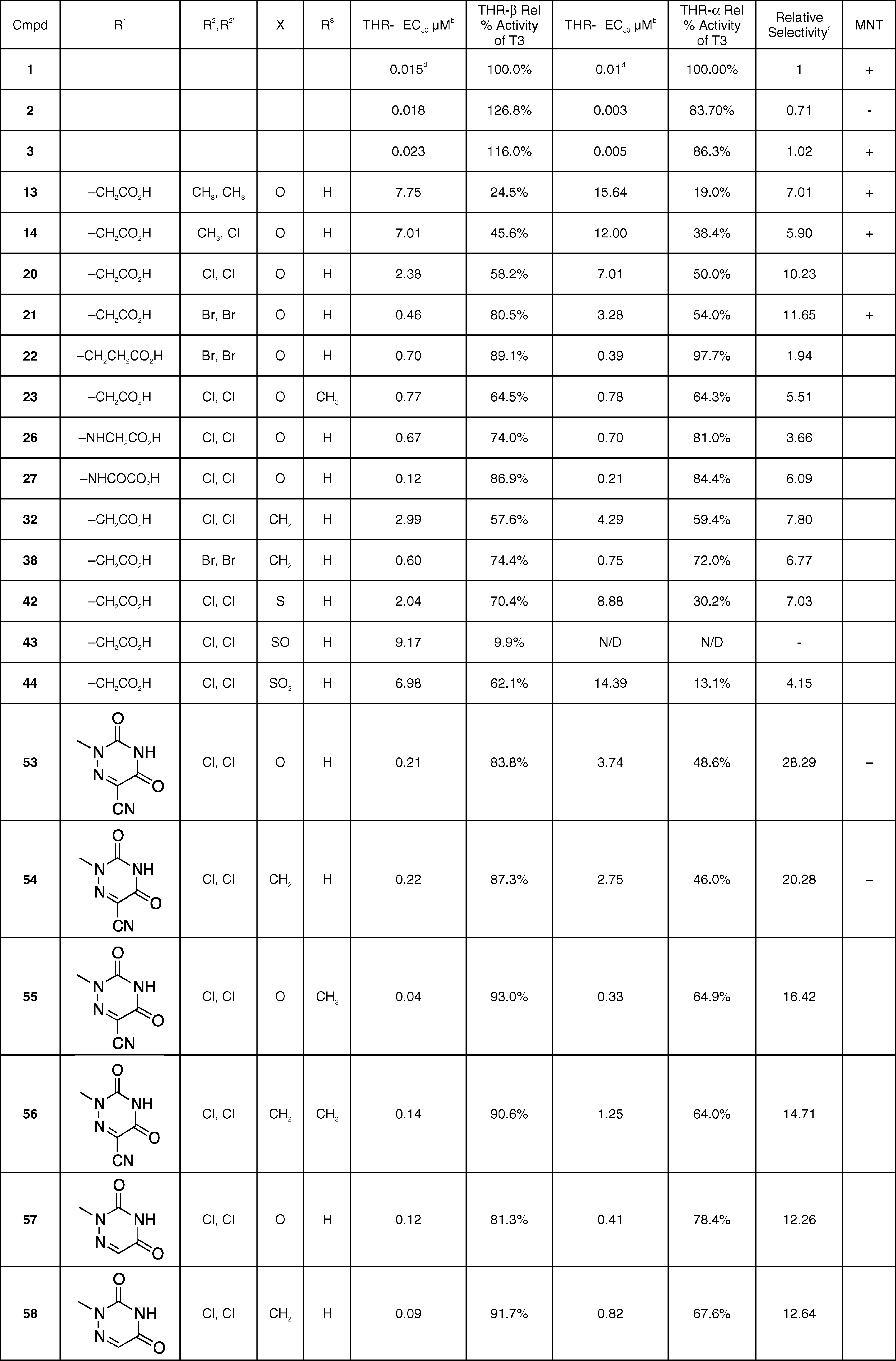
由于THRα和THRβ受体的配体结合域仅有一个氨基酸不同 天冬酰胺(Asn)331(THR-β)/丝氨酸(Ser277)(THR-α),因此筛选选择性THR-β激动剂主要集中寻找T3(化合物1)的类似物(化合物2-8)。
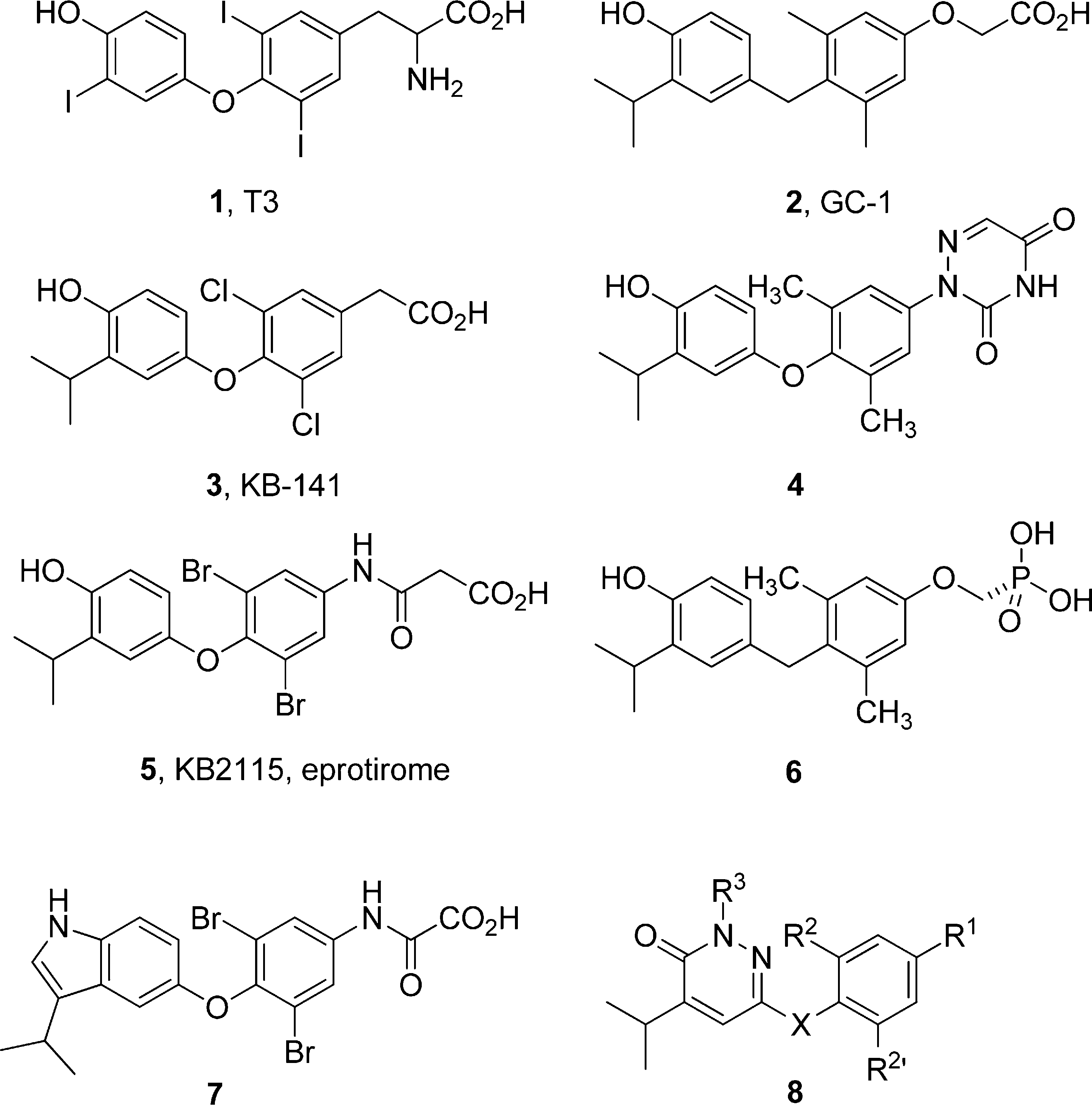
2003年Gary J Grover等人报道,使用异丙基替换T3左侧的碘苯氧中的I,使用Cl替换中间2碘苯基中的两个I,以及使用乙酸基替换右侧的2氨基-丙酸结构后,得到THR-β激动剂KB-141(化合物3)。KB-141与人THRβ的亲和性是人THRα的14倍(Gary J Grover., 2003)。
Gary J Grover又在2003年12月报道,使用甲基替换KB-141中的两个Cl,使用亚甲基替换两个苯环中间链接子O,以及在右侧苯环使用O来连接乙酸得到THR-β激动剂GC-1。GC-1与T3相比增加代谢的选择性约为引起心动过速的10的倍(Gary J Grover., 2003)。
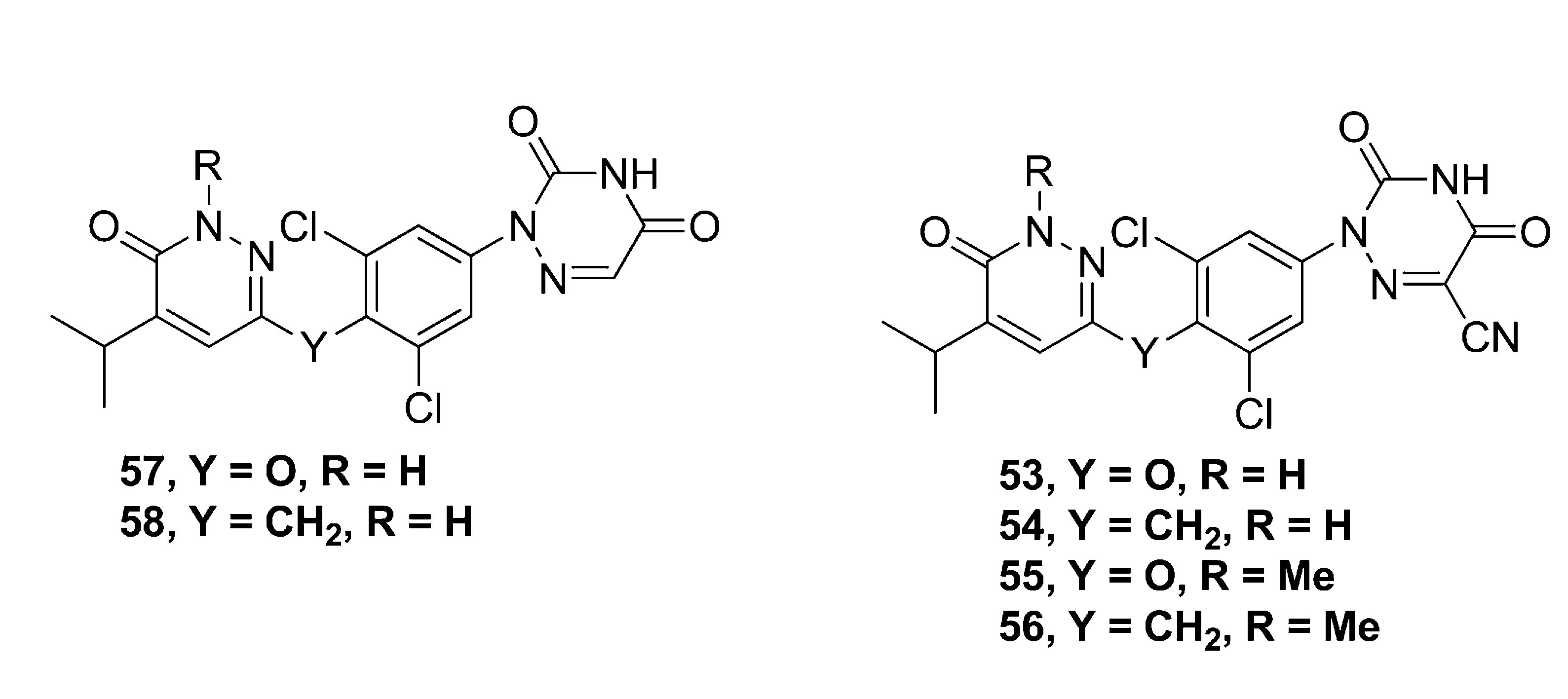
使用哒嗪酮替换3右侧的苯酚结构,得到20。20与THR-β的选择性比3高10倍,但活性却降低了100倍(Martha J Kelly., 2014)。在20的基础上使用甲基替换Cl(13和14),活性和选择性都出现稍稍下降。使用Br替换Cl,得到21。21的活性和选择性与20都得到增强。将21的乙酸基改为丙酸基(22),导会致选择性下降。使用亚甲基替换两个苯环中间的链接子O(32,38),活性基本不变,选择性降低。使用S、亚砜和砜作为链接子同样会造成选择性下降(42-44)。尽管21的活性和选择性高于20,但考虑到芳香族溴化物存在安全性风险,主要对20进行优化。将20的乙酸基改为氨基乙酸或氨基草酸的类似物(26和27),药物活性增强,但选择性下降。替换为杂氮尿嘧啶,活性显著增强,选择性略有提高(57)。在杂氮尿嘧啶上增加氰基,与57相比,尽管活性略有下降,但选择性大幅度提高(53,MGL-3196)。
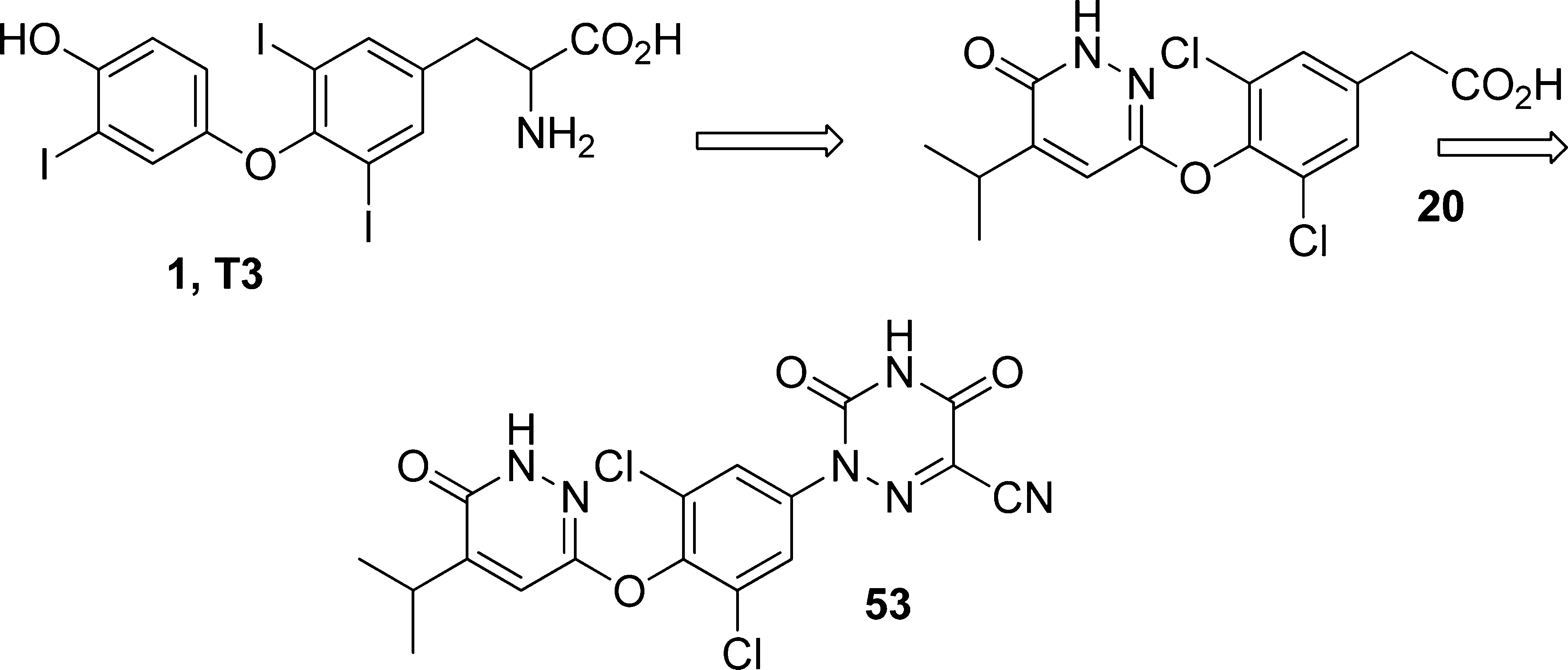
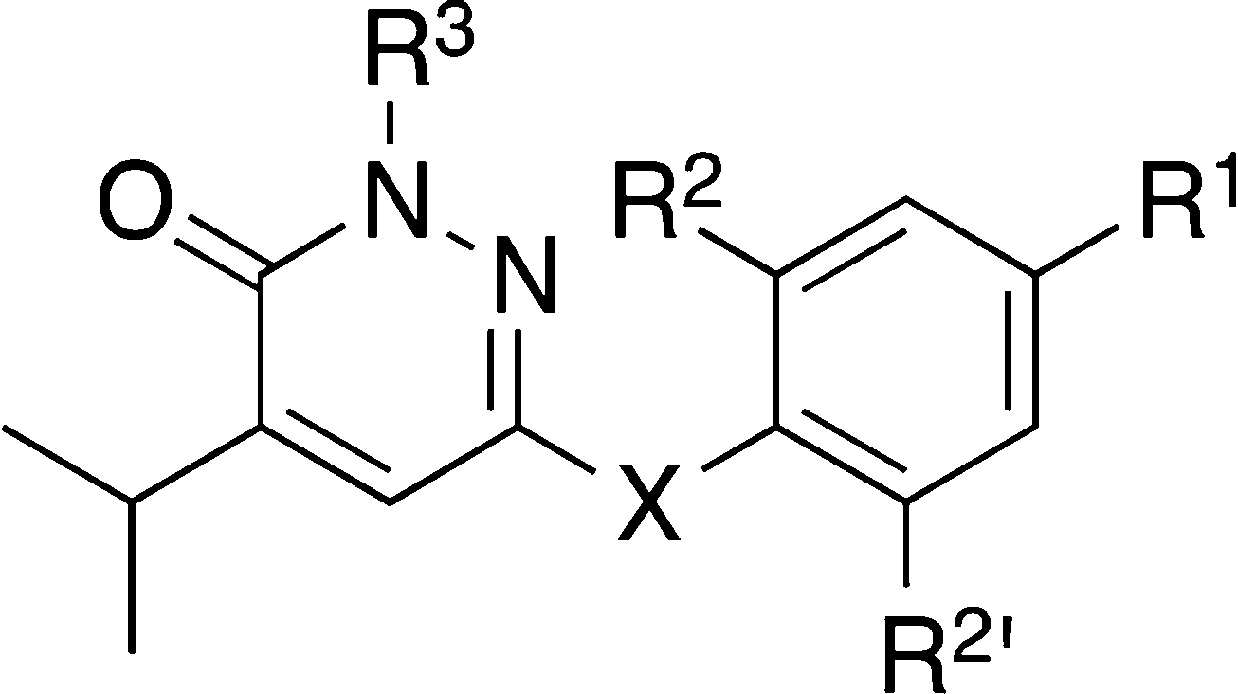
Resmetirom的1期临床试验,共纳入48名轻度低密度脂蛋白升高的健康受试者,治疗14天。结果显示MGL-3196(Resmetirom)安全性良好,各剂量组(每天5、20、50、80、100 和 200 mg)未出现剂量相关性不良事件,以及肝酶、心电图(ECG)或生命体征改变。在最高剂量,组游离甲状腺素(T4)降幅超过20%,被认为与促进T4的代谢有关。各剂量组促甲状腺素(TSH)、游离T3,及甲状腺轴功能障碍都没有了现变化。此外,在降低低密度脂蛋白胆固醇(LDL-C)方面,各剂量组最高达到30%(0.05-<0.0001),非高密度脂蛋白胆固醇达到28%(p= 0.027-0.0001),载脂蛋白B达到24%(p= 0.008-0.0004),甘油三酯(TG)达到60%(p=0.13-0.016)(Rebecca Taub., 2013)。

Resmetirom的3期临床试验(MAESTRO-NASH),共纳入1759非酒精性脂肪性肝炎(NASH)伴肝活检证实肝纤维化F1B-F3期患者按1:1:1随机分组,接受Resmetirom一天一次100mg、80mg或安慰剂治疗52周。试验结果初步分析共纳入966名患者,结果显示100mg及50mg剂量组NASH痊愈伴肝纤维化未发生恶化的比例分别为29.9%和 25.9%,显著高于安慰剂组(9.7%,P<0.001)。肝纤维化至少改善1期并且NAFLD(非酒精性脂肪性肝病)活动评分未发生恶化的比例分别为25.9%和24.2%,同样显著高于安慰剂组(14.2%,P<0.001)。第24周与基线相比LDL-C降幅分别达到16.3%和13.6%,,而安慰剂组为仅0.1%(P<0.001)。与安慰剂组相比,Resmetirom组腹泻和恶心更常见。不同试验组严重不良事件发生率相似,80mg组为10.9%,100mg组为12.7%,安慰剂组为11.5%(Stephen A Harrison., 2024)。
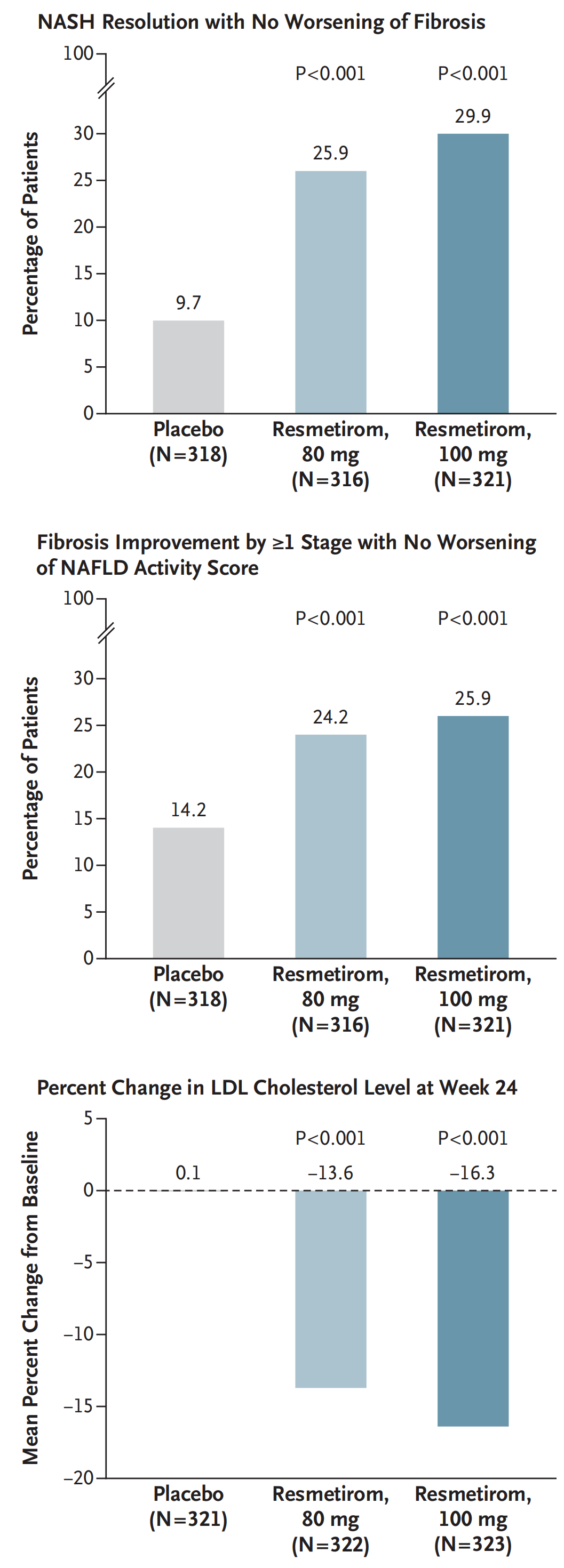
基于上述研究结果,FDA于 2024年3月14日加速审批Resmetirom用于治疗伴有轻至中度肝纤维化的NASH。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3