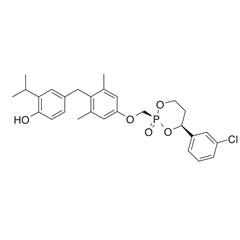
VK2809是前体药物,在肝脏内通过CYP3AA代谢酶释放出活化产物MB07344,从而实现MB07344在肝脏内活化,并选择性激动肝脏THRβ,促进肝内脂肪代谢,并减少对于肝脏以外的不良影响。
结构:
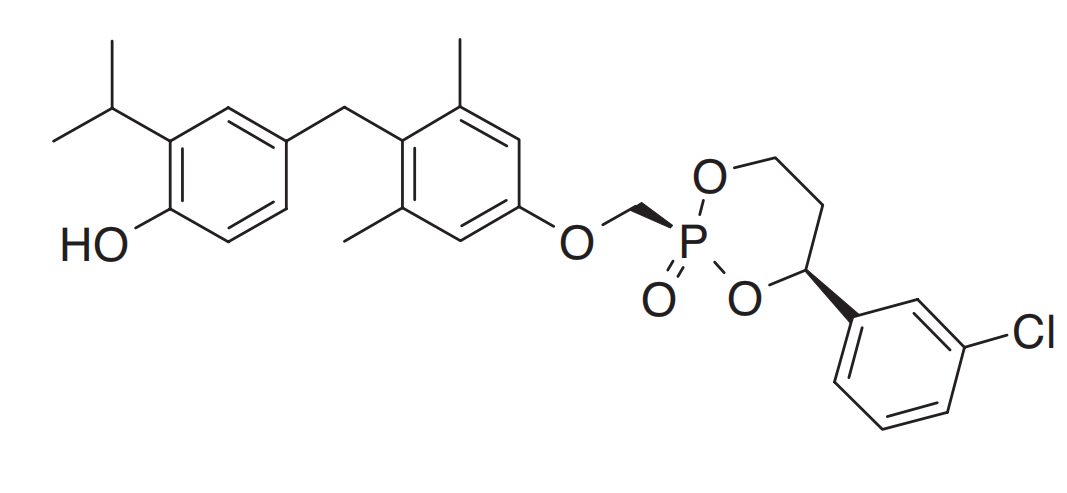
介绍:
VK2809原是Metabasis Therapeutics开发的选择性THRβ激动剂类药物(研发编号MB07811)。2009年Metabasis被Ligand Pharmaceuticals收购。2014年Viking Therapeutics从Ligand获得VK2809的开发权利。
Metabasis开发MB07811最初是希望通过引入磷酸基实现THRβ激动剂能够特异靶向肝脏,促进肝内脂肪代谢,并减少对于肝脏以外的不良影响。因此在原有THRβ激动剂(2-5)的基础上,合成出一系列含有磷酸基的结构类似物(13、15、22a-f、27、29、32、38a-c、40、45、48、57a-c、61a-b、67)(Serge H Boyer., 2008)。

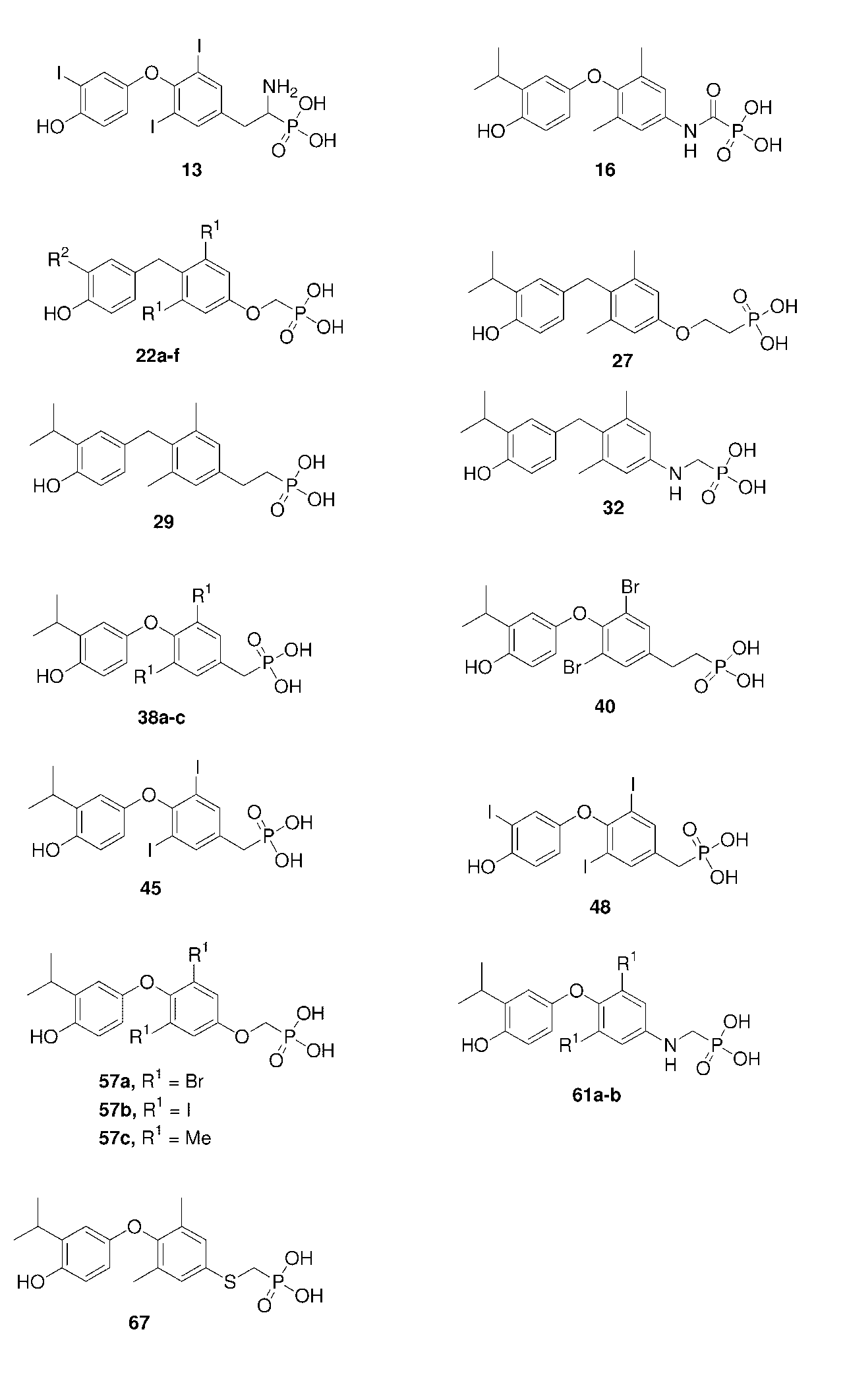
体外筛选显示22c(MB07344)具有良好的活性和THRβ选择性。
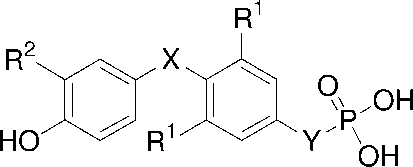
| compd | R1 | R2 | X | Y | TRα1 Ki | TRβ1 Ki |
| 1b | 0.33 | 0.68 | ||||
| 2 | 0.51 | 0.47 | ||||
| 3 | 1.09 | 0.32 | ||||
| 4 | 7.79 | 0.24 | ||||
| 13 | I | I | O | CH2CH(NH2) | 1416 | 271 |
| 16 | Me | i-Pr | O | NHCO | 285 | 36.0 |
| 22a | Me | Me | CH2 | OCH2 | 897 | 89.7 |
| 22b | Me | Et | CH2 | OCH2 | 61.6 | 9.72 |
| 22c | Me | i-Pr | CH2 | OCH2 | 35.2 | 2.95 |
| 22d | Me | Ph | CH2 | OCH2 | 1165 | 106 |
| 22e | Me | s-Bu | CH2 | OCH2 | 30.5 | 6.64 |
| 22f | OMe | i-Pr | CH2 | OCH2 | 3296 | 146 |
| 27 | Me | i-Pr | CH2 | OCH2CH2 | 594 | 87.0 |
| 29 | Me | i-Pr | CH2 | CH2CH2 | 378 | 31.3 |
| 32 | Me | i-Pr | CH2 | NHCH2 | 28.4 | 9.10 |
| 38a | Me | i-Pr | O | CH2 | 1760 | 128 |
| 38b | Cl | i-Pr | O | CH2 | 303 | 52.3 |
| 38c | Br | i-Pr | O | CH2 | 235 | 15.5 |
| 40 | Br | i-Pr | O | CH2CH2 | 42.1 | 2.50 |
| 45 | I | i-Pr | O | CH2 | 1.84 | 0.84 |
| 48 | I | I | O | CH2 | 16.0 | 26.0 |
| 57a | Br | i-Pr | O | OCH2 | 18.6 | 2.51 |
| 57b | I | i-Pr | O | OCH2 | 3.74 | 0.97 |
| 57c | Me | i-Pr | O | OCH2 | 183 | 25.4 |
| 61a | Cl | i-Pr | O | NHCH2 | 186 | 30.5 |
| 61b | Br | i-Pr | O | NHCH2 | 10.3 | 1.51 |
| 67 | Me | i-Pr | O | SCH2 | 143 | 42.1 |
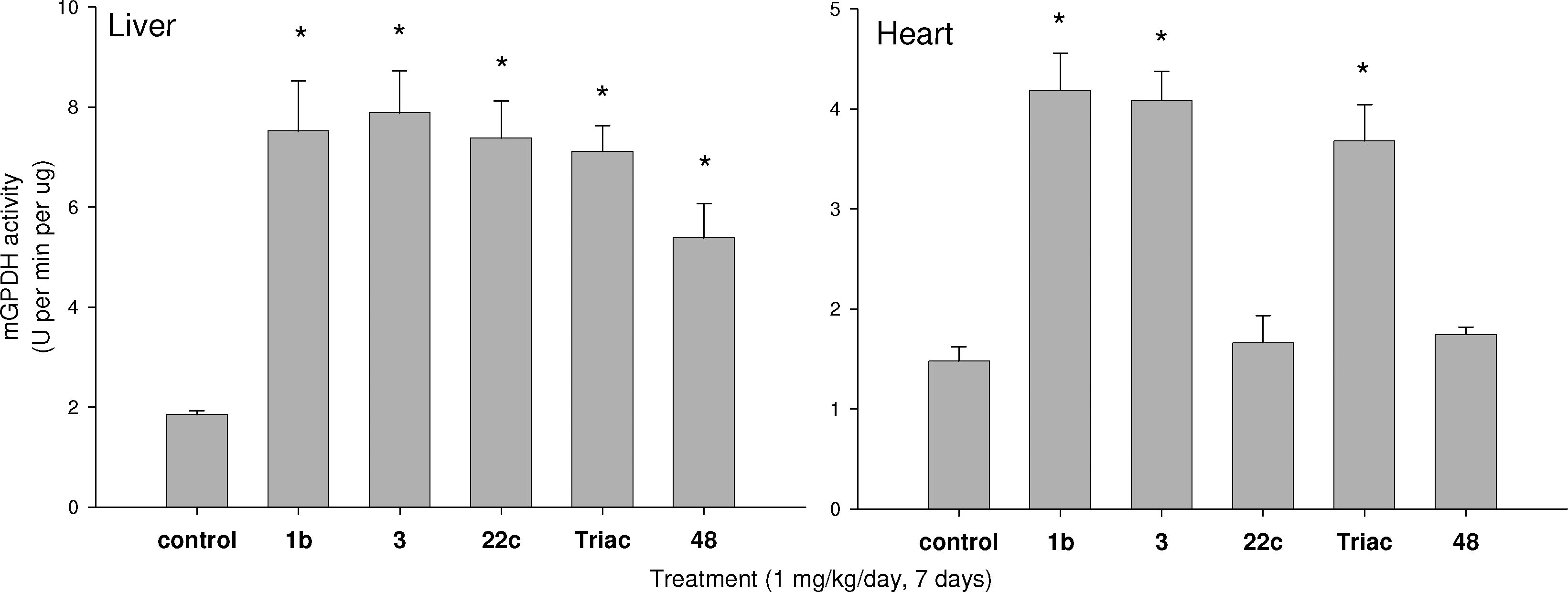
对试验动物mGPDH(甘油磷酸脱氢酶)影响的试验显示,22c(MB07344)显著增强肝脏mGPDH的活性,对心脏mGPDH未发生显著影响。
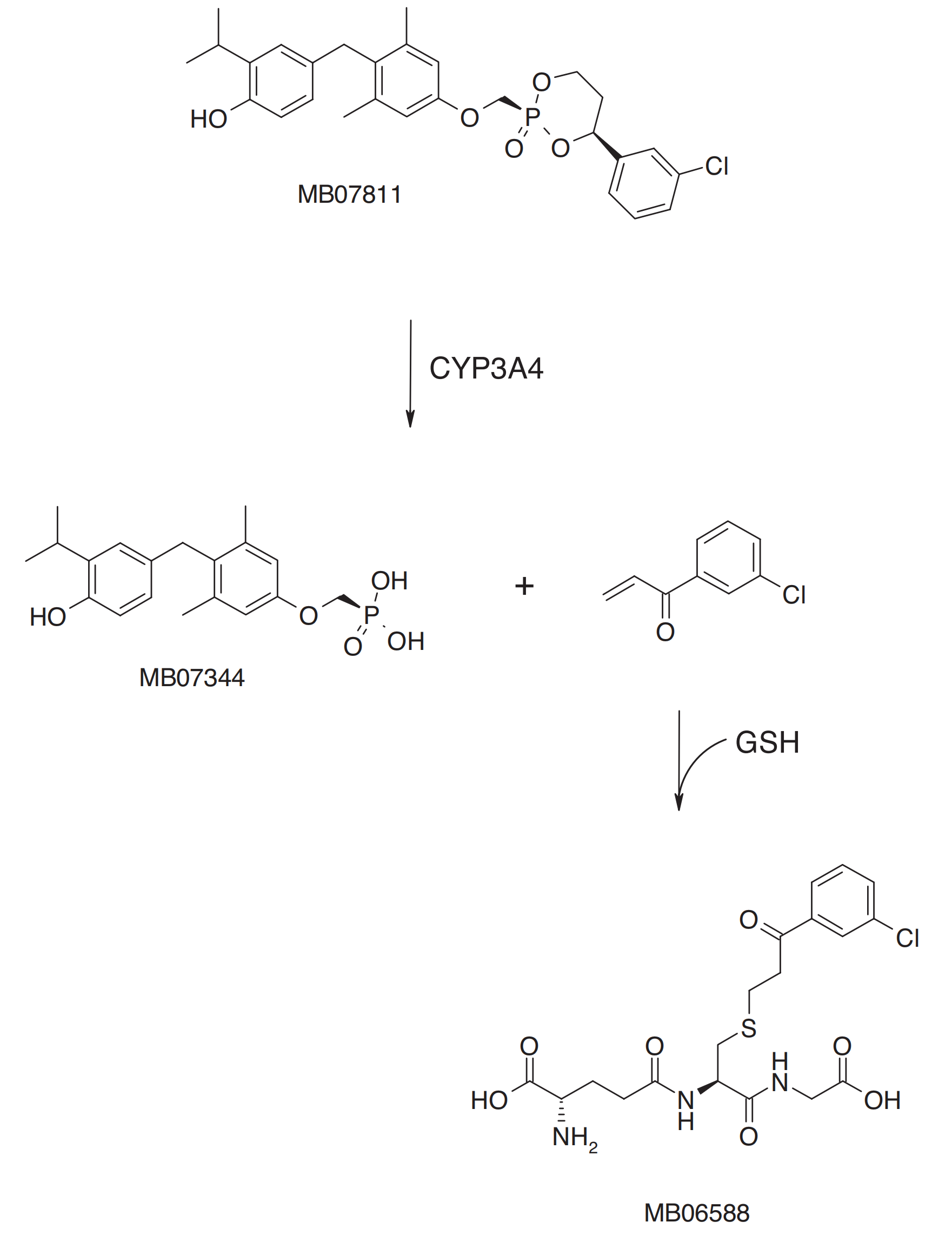
由于动物实验显示MB07344的口服生物利用度较差,使用HepDirect前药技术得到MB07811(VK2809)。HepDirect前药技术利用肝脏CYP3AA代谢酶释放出活化产物,并利GSH((谷胱甘肽)清除副产品,从而实现MB07344定向在肝脏内活化(James M Fujitaki., 2008)。
2023年11月13,Viking Therapeutics公布VK2809治疗非酒精脂肪性肝炎(NASH)2b期临床试验VOYAGE,第12 周试验结果。MRI-PDFF显示VK2809 1mg(QD)、2.5mg(QD)、5mg(QOD)、10mg(QOD)和安慰剂组肝内脂肪平均减少16.6%(p=0.082)、45.3%(p<0.0001)、36.8%(p<0.0001)、51.7%(p<0.0001)和3.7 %,组织检查显示肝内脂肪平均减少(Viking Therapeutics., 2023)。
VOYAGE是一项多中心、随机、双盲、安慰剂对照2b临床研究,用于评估VK2809治疗NASH伴纤维化的有效性、安全性和耐受性。入组包括通过MRI-PDFF测量的肝脏脂肪含量至少为 8%且肝纤维化为F2和F3期,或肝纤维化为F1期且合并糖尿病、肥胖或高血压等风险因素。该研究的主要终点为从基线到第12周肝脏脂肪含量变化,次要终点为第52 周肝活检评估肝组织学变化情况。
2024年6月4日,Viking Therapeutics公布VK2809治疗非酒精脂肪性肝炎(NASH)2b期临床试验VOYAGE,第52 周肝组织学检查结果。VK2809各剂量组NASH消退且纤维化无恶化比例为63%至75%。安慰剂组为29%(VK2809各剂量组p均<0.05)。VK2809组整体NASH消退且纤维化无恶化比例为69%(p<0.0001)。NASH消退定义为非酒精性脂肪性肝病活动评分(NAS)中为炎症评分为0或1,气球样变评分为0。VK2809各剂量组NASH无恶化且纤维化改善的比例为44%至57%,而安慰剂组为34%(VK2809 5mg和10mg剂量组p<0.05),VK2809组整体NASH无恶化,纤维化改善比例为51%(p=0.03)。纤维化改善而NASH没有恶化被定义为纤维化改善≥1期,并且NAS气球样变、炎症或脂肪变性没有恶化。VK2809各剂量组NASH消退且纤维化改善的比例40%至50%的,而安慰剂组为20%(5mg和10mg 剂量组p<0.05)。K2809组整体NASH消退且纤维化改善比例为44%(p=0.003)(Viking Therapeutics., 2023)。
|
|
Placebo (n = 41) |
VK2809 1 mg QD (n = 14) |
VK2809 2.5 mg QD (n = 52) |
VK2809 5 mg QOD (n = 27) |
VK2809 10 mg QOD (n = 44) |
VK2809 (n=137) |
|
Resolution of |
29.3 % |
71.4% (p=0.0215) |
65.4% (p=0.0023) |
63.0% (p=0.0091) |
75.0% (p=0.0001) |
68.6% (p<0.0001) |
|
Fibrosis |
34.1 % |
57.1% (p=0.1543) |
44.2% (p=0.4414) |
51.9% (p=0.0304) |
56.8% (p=0.0497) |
51.1% (p=0.0308) |
|
Resolution of |
19.5 % |
50.0% (p=0.0856) |
40.4% (p=0.0508) |
40.7% (p=0.0206) |
47.7% (p=0.0115) |
43.8% (p=0.0032) |
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3