
Vanutide Cridificar(ACC-001)由Janssen AI开发的,将Aβ42的N端序列1-7位偶合到CRM 197载体蛋白,并加入QS-21免疫佐剂制备而成的阿尔茨海默症(AD)免疫治疗疫苗。由于二期临床试验未能证实在改善AD影像学、生物标志物、及认知功能方面优于安慰剂对照组,目前已经停止开发。
结构:
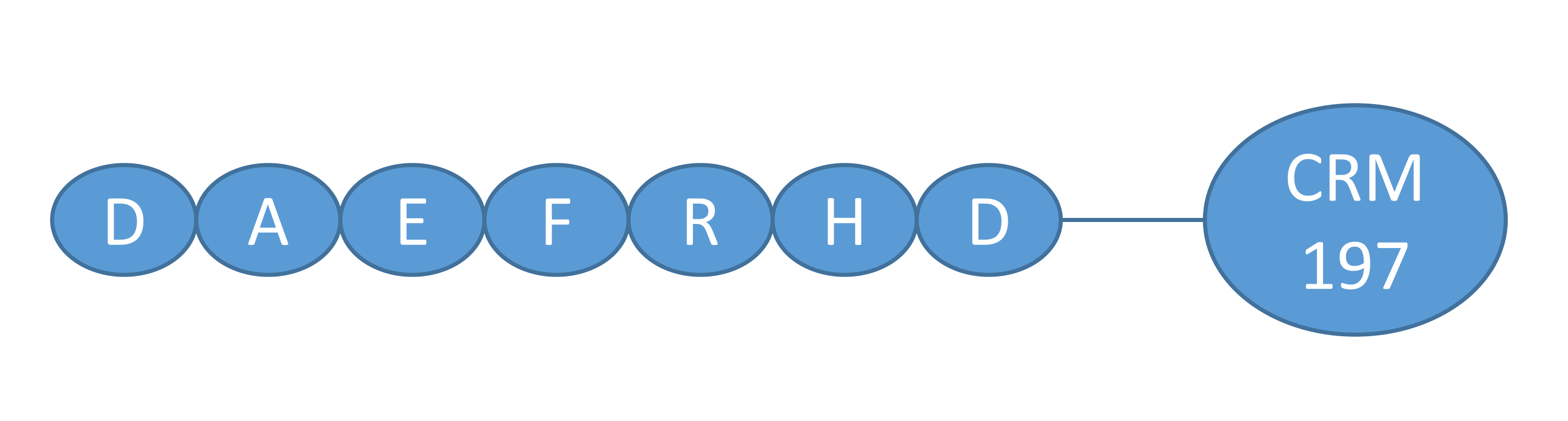
介绍:
Elan公司的AN-1792,是第一个进入临床研究的阿尔茨海默症(AD)治疗疫苗药物。在部分受试者出现 T淋巴细胞脑膜脑炎,导致AN-1792项目失败后,Elan公司着手开发不激活T淋巴细胞的AD免疫治疗药物。一个技术方向是开发缺少T淋巴细胞结合位点的治疗性疫苗。另一个技术方向是开发靶向β淀粉样蛋白斑块的单克隆抗体。
疫苗属于主动免疫,单克隆抗体为被动免疫。相比单克隆抗体,疫苗的开发周期更短,成本更低,也不需要维持用药。
2003美国哈佛大学医学院布列根和妇女医院的Alon Monsonego在8月期《The Journal of Clinical Investigation》上发表的论文显示,T淋巴细胞主要结合于Aβ的16-33位。2005年Elan公司的Dale Schenk团队在9月期《Neurology》上发表的论文显示,AN-1792接种者产生的抗体主要识别β淀粉样蛋白多肽42(Aβ42)的N端序列1-8位,提示Aβ42的N端序列可单独用于开发不激活T细胞的AD治疗疫苗。由于Aβ42的N端序列长度比较短,难以激活B细胞产生抗体,因此需要在Aβ42的N端序列的基础上接入其他结构。
ACC-001是Aβ42的N端序列1-7位偶合到CRM 197载体蛋白,并加入QS-21免疫佐剂制备而成的AD免疫疫苗。CRM 197载体蛋白为白喉毒素无毒突变蛋,常用于与免疫抗原结合,以便形成稳定的抗体。QS-21来源于从南美皂树树皮中的皂苷,可增强机体对接种抗原的免疫反应。
2007年11月和4月Elan和Wyeth-Ayerst惠氏在欧洲和美国启动了ACC-001的二期临床试验。由于一例德国患者出现严重的皮肤损害,ACC-001项目被暂时中止。2008年5月,美国FDA在审查ACC-001的安全性数据后,批准恢复了ACC-001的临床试验。
2009年Elan将其AD免疫治疗药物研发管线全部出售给Johnson & Johnson强生旗下新成立的Janssen Alzheimer Immunotherapy Research & Development, LLC.(杨森阿尔茨海默症免疫治疗研发公司,Janssen AI)。而Pfizer辉瑞也完成了对Wyeth的收购。在收购完成后,Janssen AI和Pfizer继续推进ACC-001(Vanutide Cridificar)的二期临床试验。
2016-2017年发表的多篇ACC-001二期临床研究试验结果,均未能证实ACC-001在改善AD影像学、生物标志物、及认知功能方面优于安慰剂对照组,ACC-001的研究项目随之终止。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3