
呋喹替尼为口服小分子VEGFR-1、-2及-3选择性抑制剂。
结构:
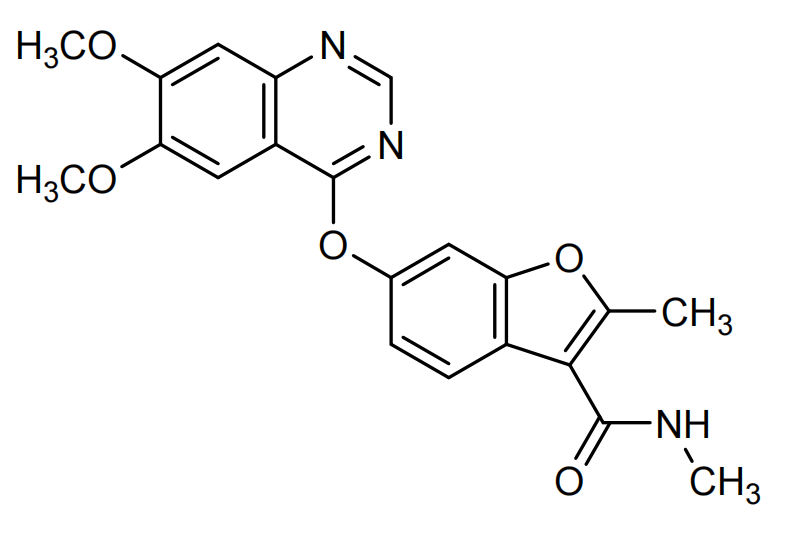
介绍:
呋喹替尼(Fruquintinib,商品名:爱优特Elunate/Fruzaqla;研发代号:HMPL-013)是和黄医药HUTCHMED开发的口服小分子VEGFR-1、-2及-3选择性抑制剂。
| Kinase assay | IC50 (nmol/L) or Inhibition rate (%) |
| VEGFR2 (KDR) | 35* (25) |
| VEGFR3 (Flt4) | 0.5* |
| VEGFR1(Flt1) | 33* |
| Ret | 128* |
| FGFR1 | 181* |
| c-kit | 458* |
| Flt3 | >10000 |
| PDGFRβ | >10000 |
| EGFR | >30000 |
| Tie2 | >10000 |
| c-Met | >10000 |
| EphB4 | >3000 |
| Akt | >3000 |
| CHK1 | >10000 |
| CDK1 | >10000 |
| CDK2 | >10000 |
| CDK5 | >10000 |
2018年,Jin Li等人发表呋喹替尼用于既往接受过治疗的转移性结直肠癌患者3期临床试验FRESCO的研究结果。该研究共纳入国内28个中心,416名转移性结直肠癌患。患者按2:1的比例随机接受呋喹替尼5mg(n = 278)或安慰剂(n = 138),口服每日一次,持续 21 天,随后停药7天。以28 天为周期,直至疾病进展、出现无法耐受的毒性或退出研究。研究结果显示与安慰剂相比,呋喹替尼显著延长的中位数总生存期(9.3个月 [95% CI,8.2-10.5] vs 6.6个月 [95% CI,5.9-8.1]);死亡风险比(HR)=0.65(95% CI,0.51-0.83;P < .001)。与安慰剂相比,呋喹替尼组的中位数无进展生存期也显著增加(3.7个月 [95% CI,3.7-4.6] vs 1.8个月 [95% CI,1.8-1.8]个月);进展或死亡HR=0.26(95% CI,0.21 -0.34;P < .001)。在治疗期间61.2%(170例)接受呋喹替尼治疗的患者发生3-4 级不良事件,安慰剂组为 19.7%(27例)。呋喹替尼组15.5%(43例)的患者报告了严重不良事件,安慰剂组为5.8%(8例)的患者报告了严重不良事件,其中 14.4%(40例) 接受了呋喹替尼治疗的患者和 5.1% (7例)接受安慰剂治疗患者需要住院治疗(Jin Li., 2018)。
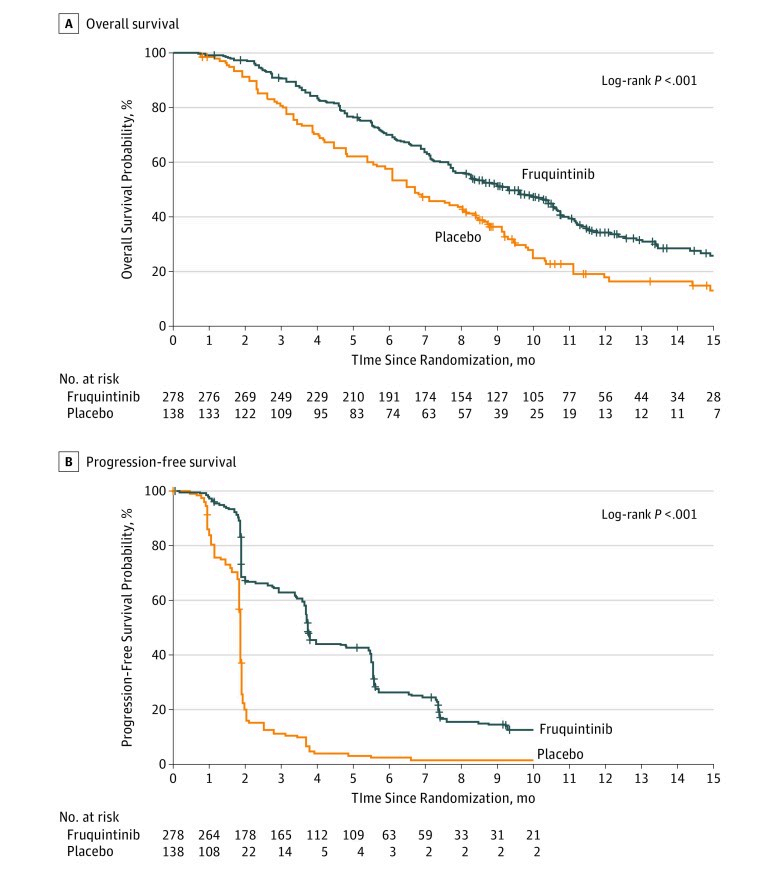
2018年呋喹替尼(Fruquintinib,商品名:爱优特Elunate)在国内批准单药适用于既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子(VEGF)治疗、抗表皮生长因子受体(EGFR)治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
2023年01月23日,和黄医药宣布与武田(Takeda)制药与黄医药达成合成协议,以及4亿美元首付款,最高7.3亿美元的潜在里程碑付款,以及于基于净销售额的特许权使用费的形式,武田获得在除中国内地、香港和澳门以外的全球范围内推进呋喹替尼开发、商业化和生产权利(和黄., 2023)。
2023年,Arvind Dasari等人发表呋喹替尼用于难治性转移性结直肠癌3期临床试验FRESCO-2的研究结果。该研究共纳入14个国家、124个中心,691名患者。患者按2:1的比例随机接受呋喹替尼5mg(n = 461)或安慰剂(n =230),口服每日一次,持续 21 天,随后停药7天。以28 天为1个周期。研究结果显示呋喹替尼组中位数总生存期为7.4个月(95% CI 6·7-8·2),安慰剂组为4.8个月(4.0-5.8)(HR= 0.66,95% CI 0.55-0.80;p<0.0001)。接受呋喹替尼治疗的456 例患者中有286例 (63%)发生3级或更严重不良事件,接受安慰剂治疗的 230 例患者中有 116 例(50%) 发生3级或更严重不良事件。呋喹替尼组最常见的 3 级或更严重不良事件包括高血压(n=62 [14%])、乏力(n=35 [8%])和手足综合征(n=29 [6%])。每组有 1 例治疗相关死亡病例(呋喹替尼组为肠穿孔,安慰剂组为心脏骤停)(Arvind Dasari., 2023)。
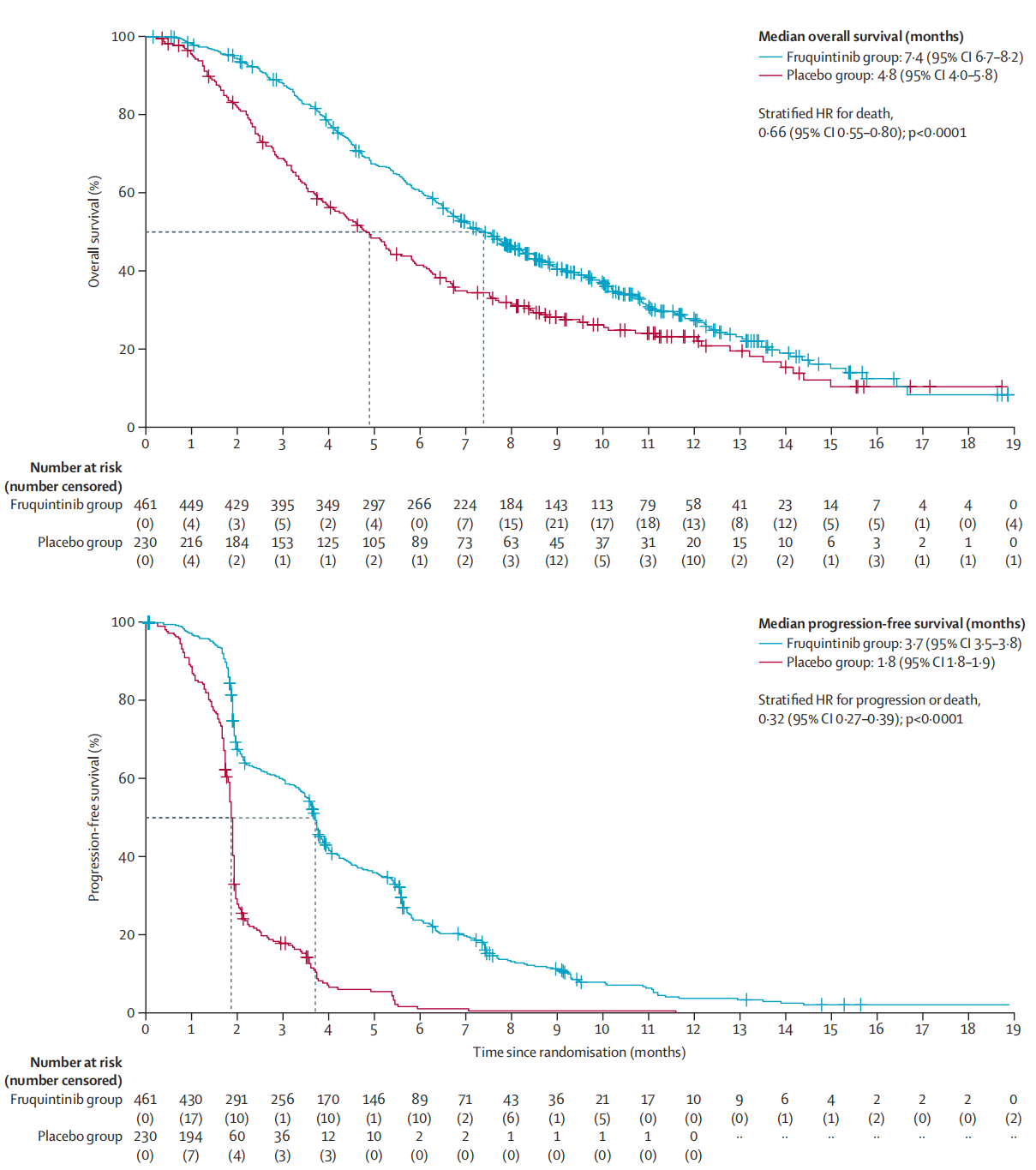
2023年11月8日,武田(Takeda)宣布呋喹替尼(Fruquintinib,商品名:FRUZAQLA)获得美国食品药品监督管理局(FDA))批准,用于治疗既往接受过氟尿嘧啶、奥沙利铂和伊立替康基础的化疗,抗VEGF治疗以及RAS野生型且医学上合适的抗EGFR治疗的成人转移性结直肠癌(Takeda., 2023)。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3