降压药物的出现显著降低了心、脑、肾等相关疾病的死亡风险,能够实现更好管理血压,成为抗高血压药物筛选的主要目标。
1733年英国的Stephen Hales使用9英尺的玻璃管插入马的小腿动脉。当玻璃管内血液爬升到8英尺3英寸后,开始以连续的周期性在上下3英寸的幅度内上升和下降。第一次,Stephen Hales实现测量血压(BP)。

而使用玻璃管测量血压这一方法的正式建立,实际上基于Harvey同时代的荷兰人Daniel Bernoulli于1738年出版的著作《流体动力学》。此后近百年的时间,医生都用玻璃管来测量血压。玻璃管需要插入动脉,结果也经常不准,并不具有临床实际的应用价值。1828年法国人Jean Léonard Marie Poiseuille发明了U型水银血压计。Poiseuille将玻璃管接入装有水银的U型管,利用血液推动水银导致U型管两侧水银液面高度出现差值来计量血压。
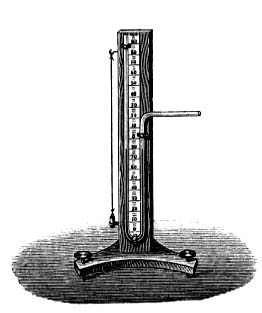
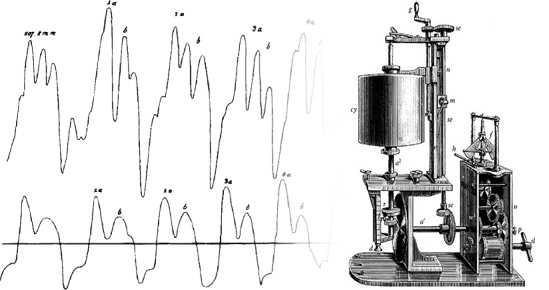
1847年德国人Carl Ludwig将Poiseuille的U型水银血压计和滚筒以及记录笔连接,称之脉搏描记器(kymograph)。滚筒由时钟驱动,记录笔可以随着银水柱变化来回移动在滚筒上进行记录。Ludwig还使用脉搏描记器的记录来描述窦性心律失常。Ludwig的发明首次实现计录血压周期性变化,但仍旧属于侵入性的测量方法,直到1856年法国人Jean Faivre通过将Poiseuille的装置插入一名截肢男性的股动脉才第一次获得人体血压的读数,其测得股动脉的血压为120mmHg。
由于侵入性的测量血压,不具有实际普通应用的意义,因此对于高血压的最初认识,并不是来自于实际测量血压,而是基于慢性肾脏病(CKD)患者出现左心室肥大的病理推断。
肾脏病源于发现蛋白尿。1527年德裔瑞士医生和炼金术士Paracelsus在一次讲座中,提出他对于消化的认识。 Paracelsus认为食物从胃开始消化、然后是肝脏、然后是肾脏,每一步都会进行转化,到达肾脏时食物变成乳白色。如果肾脏消化功能失效,乳白色的食物便会从尿液中排出。Paracelsus介绍了一个在尿液中排出“牛奶”的乞丐,在他的尿液加入葡萄酒或醋后,尿液会出现凝固物,放置几天后,在尿液表面可以看到漂有类似奶油的油花。
1694年荷兰人Frederick Dekkers出版一本关于治疗学的著作。在Dekkers的著作中也记录了“牛奶”尿。Dekkers提到这些尿液在加热会变成“牛奶”,闻起来像“牛奶”,尝起来像甜“牛奶”,如果向尿液滴一两滴醋酸,放置在清凉处会产生,不久就会形成白色的沉淀,尿液表面会漂浮油状物。Dekkers推测这种尿液是清澈的乳糜,也可以说是一种营养液。
1765年意大利人Domenico Cotugno记录一名28岁之后被认为是猩红热的患者。患者出间歇性的发热、5天后开始出现水肿和少尿,给患者使用利尿剂后,一晚上患者就能排出10-12品托(英制体积单位1 品脱≈568ml)的尿液。Cotugno认为患者是体液紊乱的结果,因此蒸发了患者的尿液,蒸发不到一半,尿液便凝结成白色凝固物,类似于蛋鸡清凝结成蛋鸡白。
1797年、1798、1806年英国军医John Rollo发表了3版对糖尿病的论著。其在好友William Cruickshank的帮助下对患者尿中的“糖”进行了定量分析。William Cruickshank发现一些出现水肿患者的尿液在加热后会出现白色沉淀,这些尿液的性质与血清非常接近,此外William Cruickshank还发现这类患者会出现血尿。
1827年英国人Richard Bright出版关于肾病的《病例集》,他注意到肾病患者常出现水肿、蛋白尿和肾脏病理变化,之后把具有这种“三联征”的疾病称为布莱特氏(Bright)病。在Bright的《病例集》中,详细计录一例肾病伴有左心室肥大的病例。尽管Bright并不确定,他猜测左心室肥大源于循环系统上的问题。1839年Bright和他的同事Joseph Toynbee通过显微检查发现慢性肾病(CKD)患者的动脉出现增厚,也就是现在所说的动脉硬化。
1853年Bright在英国盖伊医院(Guy’s Hospital)的继任者Samuel Wilks通过详述布莱特氏病,论述了布莱特氏病和左心室肥大之间的联系。
1856年德国人Ludwig Traube在著作《Ueber den Zusammenhang von Herz-und Nieren-krankheiten(论心肾疾病的关系)》对动脉硬化和左心室肥厚做了大胆推测,认为是长时间高张力造成的结果。在Traube的著作中,Traube承认他是推测是受英国圣巴多罗买医院(St Bartholomew's Hospital)William Senhouse Kirkes关于高动脉内压论述的影响。
1856年德国人Ludwig Traube在著作《Ueber den Zusammenhang von Herz-und Nieren-krankheiten(论心肾疾病的关系)》对动脉硬化和左心室肥厚做了大胆推测,认为是长时间高张力造成的结果。在Traube的著作中,Traube承认他是推测是受英国圣巴多罗买医院(St Bartholomew's Hospital)William Senhouse Kirkes关于高动脉内压论述的影响。
Traube的推测,让高血压这一沉默的杀手,显露出凶残的本性。高血压正式从幕后走向前台,学者们着手探索高血压的形成机制。
首先提出来是高血压源自于由肾脏的推论。1852年英国人George Johnson在他的著作中介绍观察到莱特氏病患者肾小球入球动脉出现增厚,而出球动脉正常,由此推测由于肾脏退行性病变,造成入球动脉血液中的尿液成分不能有效排出,血液不能滋养血管或对血管有害,导致肾小动脉增厚,以及左心室肥大。1868年Johnson补充了他的推论,指出肾小动脉增厚导致动脉阻力增加,进而引起左心室肥大。
另一种高血压形成的理论由英国盖伊医院的William Withy Gull和Henry Sutton。他们发现慢性布莱特氏病患者不仅肾动脉出现病变,全身其它的器官的毛细血管也会出现纤维化。部分患者的肾脏萎缩并不严重,但仍可见全身毛细血管纤维化。因此Gull和Sutton认为全身毛细血管的病变,导致动脉阻力增加和左心室肥大(1872年)。
第三种高血压形成的理论也是来自于国盖伊医院,由Frederick Akbar Mahomed于1874提出。Mahomed是将血压测量实际应用于临床的先驱,也是把高血压列为人类最常见健康杀手的先驱。1854年德国人Karl von Vierordt通过直接给动脉施加压力,测量阻止桡动脉搏动所需的压力,实现非侵入性测量血压。1860年法国人Etienne-Jules Marey以此发明一种便携式的血压测量装置。Marey的装置实际不能精确测量血压具体的数值,而是通过一根杠杆来记录血压和脉搏变化,杠杆的一端紧靠手腕的脉搏,另一端是记录笔,可以在可移动的熏黑纸上划出痕迹。Mahomed改良了Marey的装置,使其更轻也更加灵敏,并在珠宝商的帮助下使用黄金替代装置上的金属螺钉,以便用可以盎司来计量施加的压力。
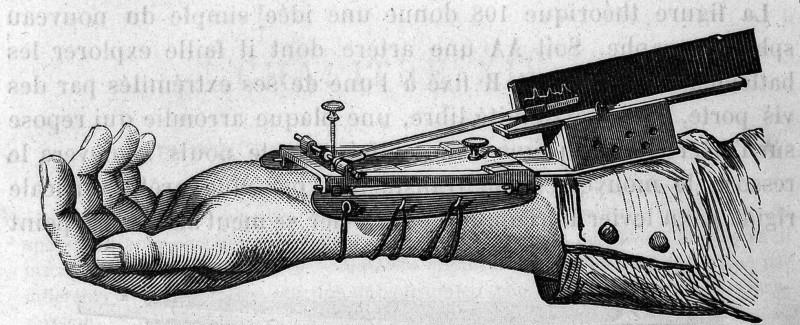
1870年至1881年,Mahomed使用其改进的装置测量了数百名各类患者的血压,根据装置记录的波形特殊判断是否存在高血压。1874年Mahomed在其专著《Etiology of Bright’s Disease and Prealbuminuric Stage莱特氏病病因学和白蛋白尿前期》中提出高血压引起莱特氏病的推测。提出在出现莱特氏病相关症状前,由于未知原因引起血压升高,未能控制的血压,导致患者出现蛋白尿。
尽管Mahomed把血压测量引入临床实践,但直到1896年意大利人Scipione Riva-Rocci发明一种易于在床边使用的带有血压袖带和水银压力计的血压计,血压测量才真正有望实现普及。Riva-Rocci的袖带水银血压计使用气球给血压袖带充气,通过感觉袖带充气或放气时脉搏消失或重新出现时水银压力计测得的压力来确定肱动脉血压。
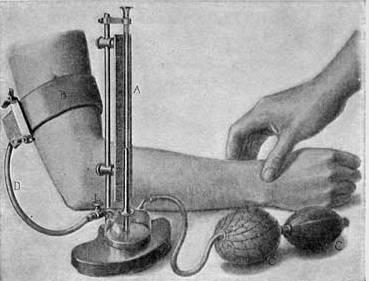
Riva-Rocci的袖带水银血压计测得的是收缩压。而收缩压得益于1905年俄罗斯人Nikolai Sergeyevich Korotkov对袖带水银血压计使用方法的改进。Korotkov将听诊器插入袖带下肱动脉搏动处,随着袖带压力下降,在听诊器中能够听到两次声音,第一次为血液恢复流动时发生的声音,此时测得的为收缩压,第二次为血液可以不受袖带约束,自由流动时发生的声音,此时测得的为舒张压。既方便又准确,袖带水银血压计的出现,为普及血压测量,扫平了最大障碍。
Riva-Rocci的袖带水银血压计测得的是收缩压。而收缩压得益于1905年俄罗斯人Nikolai Sergeyevich Korotkov对袖带水银血压计使用方法的改进。Korotkov将听诊器插入袖带下肱动脉搏动处,随着袖带压力下降,在听诊器中能够听到两次声音,第一次为血液恢复流动时发生的声音,此时测得的为收缩压,第二次为血液可以不受袖带约束,自由流动时发生的声音,此时测得的为舒张压。既方便又准确,袖带水银血压计的出现,为普及血压测量,扫平了最大障碍。除此之外,医学界先驱们的倡导以及保险公司的参与,都为普及血压测量做出了重要贡献。
1901年美国外科医生Harvey Cushing在意大利旅行期间,他的意大利同行送给了一个袖带水银血压计。回到美国后Cushing把血压计介绍给约翰斯·霍普金斯医院(Johns Hopkins Hospital)的同事使用。随后血压计引起了在纽约工作的Theodore Caldwell Janeway和克利夫兰(Cleveland)工作的George Crile的关注。Janeway、Crile、Cushing及Cushing在Hopkins的同事为成在美国使用血压计的早期倡导者。1904年Janeway总结使用经验,出版专著介绍袖带水银血压计在医疗、外科、产科领域的中应用。
1906年医学界还在争论血压计的应用价值的时候,一些寿保险公司关注到测量血压计在评估健康风险方面的重要价值,要求投保人在人寿保险体检时需要测量血压。1912年美国大都会人寿保险公司(Metropolitan Life Insurance Company)发表了相关报告,根据精算师的测算表明,拒绝血压严重异常的投保人参保,降低了参保人整体的实际死亡率。到1918年测量水压已成为美国保险业标准健康体检项目,也逐渐成了临床医生的标准程序。从1925年至1979年的一系列报告中,美国精算学会记录了以人口为基础的血压分布、与年龄相关的血压变化、以及血压与体型和死亡率之间的关系。
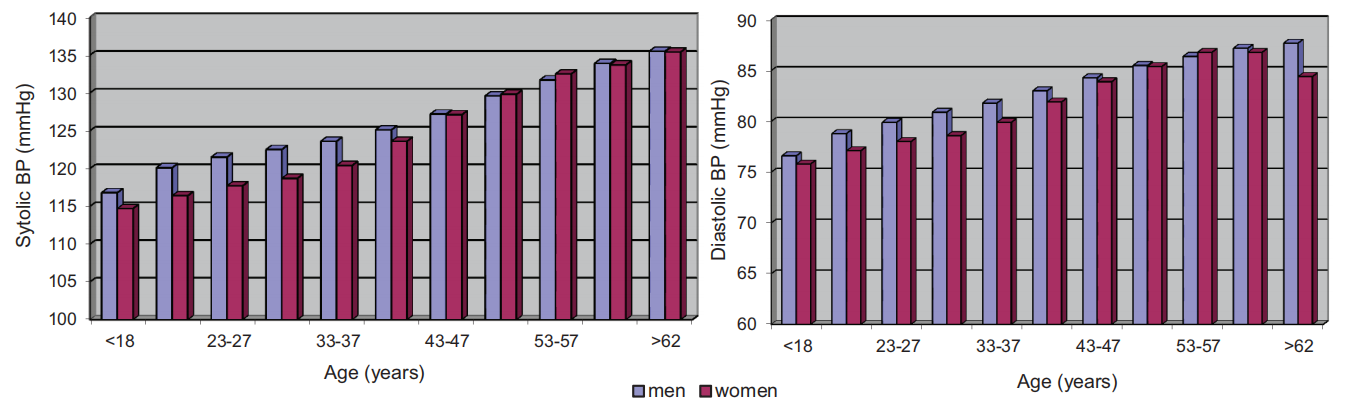
与此同时,对于慢性高血压特别是轻度慢性高血压是否应该治疗存在不同意见,一些权威人士将高血压视为对于微血管疾病的代偿性反应。1937年美国总统富兰克林·罗斯福(Franklin Roosevelt)在其54岁时测得的血压为162/98mmHg,受当时主流观念的影响,他的私人医生,未给出任何干预血压的建议。1941年,罗斯福血压达到188/105mmHg。1943年到1944年期间罗斯福开始出现心力衰竭的证据。他的医生开始使用洋地黄疗法并尝试低盐饮食,来控制心力衰竭症症状。虽然当时有一些降血压的药物可以使用,但疗效有限,并且也有潜在的严重副作用。1945年4月12日罗斯福血死于脑卒中。
与对于慢性高血压危害性的认识不同,对于恶性高血压,当时一些医生已经认识到往往意味着预后不到1年,并尝试寻找降压方法。首先考虑是饮食控制,1922年美国医生Allen和Sherrill便已经建议使用低钠饮食,但未引起足够的重视。在饮食控制方面更为成功的是Drove Kempner,Kempner设计了一天只能摄入2000卡热量的食谱来治疗一名49岁糖尿病合并高血压的患者。食谱包括大米、水果和含柠檬酸盐的果汁,钠的摄入量限制在150mg,4% - 5%的蛋白质和2%-3%的脂肪。经过Kempner的食谱治疗后,该患者的心脏充血、心电图和视网膜病变都得到了明显改善。1944年Kempner在美国医学会大会上展示该病例资料并招募更多患者。由于该病例治疗结果过于良好,导致许多在会医生认为Kempner造假,《JAMA》和《Archives of Internal Medicine》甚至拒绝发表。在支付高额的版面费后,才得以在《North Carolina Medical Journal》发表。在Kempner最初招募的192名患者中,25例患者死亡,60名患者的血压值没有明显改善,其余107例患者血压从平均200/112 mmHg降低到平均149/96 mmHg。72例患者中66例患者的心脏充血得到改善,82例患者中73例患者的血清胆固醇降低。33例患者中21例的视网膜病变减轻或完全消失。1948年Kempner的报告显示,在500名参加该项目的患者中,322名患者的血压实现下降。该方案最大的问题是患者难以坚持。Kempner也没有把降低血压的原因归结到低钠引食上。事实上Grollman在1945年就已经提出限食引起的血压下降与低钠有关。
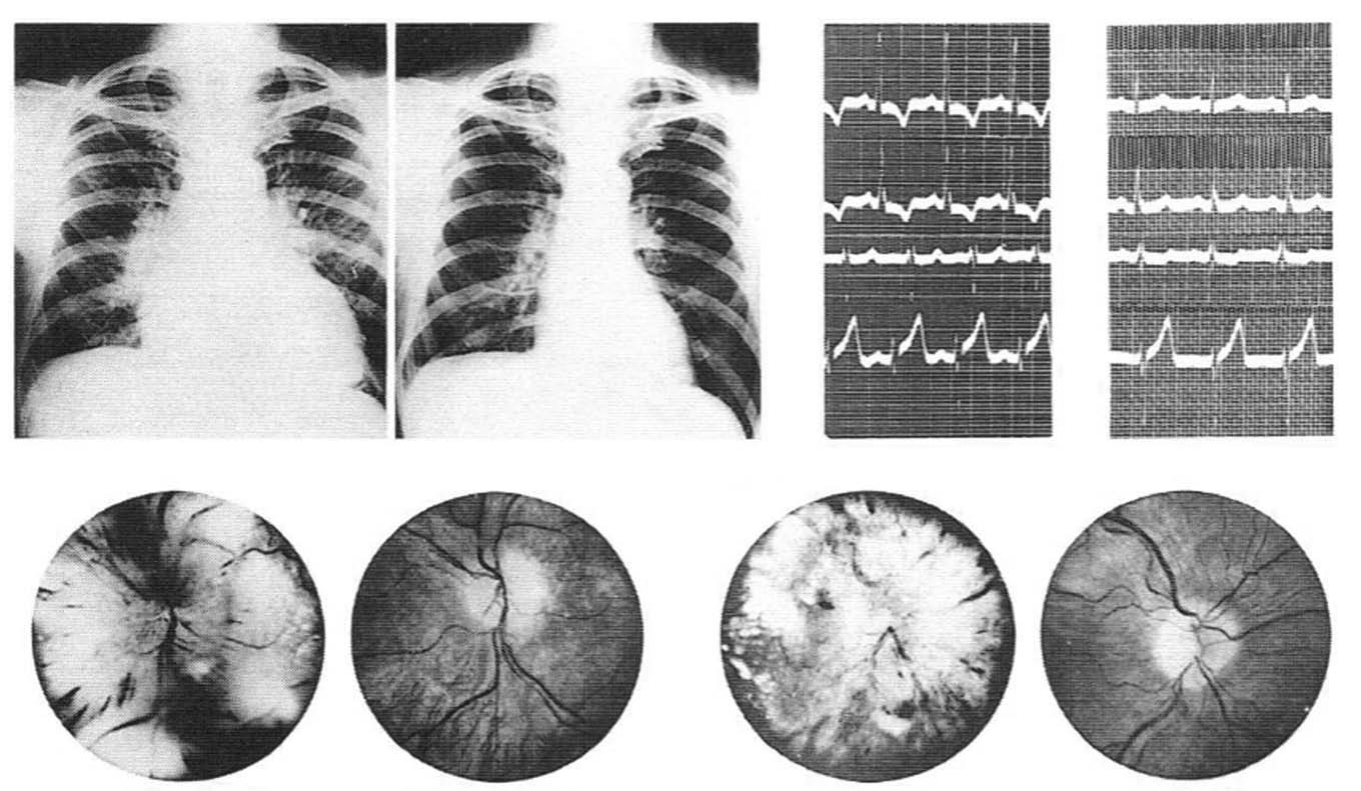
除饮食控制外,当时为了降低血压,还尝试了一些激进的方法,如注射热原和交感神经切除术。虽然交感神经切除术可以阻止40-50%患者的严重高血压发生进展,但会引起严重的直立性低血压,并且手术风险也是不得不考虑的问题。
最早用于降压的药物是硫氰酸盐,1903年Pauli将其用于治疗高血压。尽管硫氰酸盐能够显著降低血压,但也容易出现精神系统毒性反应。1940s发明了检测血液硫氰酸盐浓度的简便方法。在此之后,引入血药浓度监测来防止硫氰酸盐出现中毒性反应。硫氰酸盐一直使用到1950s。之后逐渐被其他药物替代。
另一个早期发现具有降血压的药物是硝普钠(Sodium Nitroprusside)。硝普钠于1849年由Playfair首次发现。1928年Johnson首次报道了硝普钠具有降低血压的作用。硝普钠直接扩张血管降压血压,但作用时间短,因此主要用于恶性高血压。
1931年来得印度加尔各答(Calcutta)的两名医生Gananath Sen和 Chandra Bose在《Indian Med World》上发表论文,发现印度植物萝芙木(Rauwolfia)具有降低血压的作用。1952年Műller、Schlittler和Bein在瑞士制药公司Ciba Geigy的资助下从中分离出生物碱利血平。利血平能够耗竭交感神经突触部位囊泡内的去甲肾上腺素,从而减少去甲肾上腺素的释放。由于易产生直立性高血压,目前很少使用。
1940s对于季铵盐类的生物效应进行了广泛研究,包括肌松作用以及降压作用,降压作用通常被认为是一种副作用,未引起重视。1945-1946年美国哈佛医学院(Harvard Medical School)的 George Acheson和Gordon Moe通过实验证实这类药物通过阻断神经节发挥作用,因此称之为神经节阻断药物。Acheson和Moe对四乙基铵(Tetraethylammonium,TEA)的肌松作用进行临床研究,由于该药的作用时间短,临床价值有限,在试验中TEA也表现出具有降低血的副作用。没过多久,英国家国家研究所(National Institute)的William Paton在测试地衣状菌素(Licheniformin)毒副作用过程中发现地衣状菌素能够刺激组胺释放,为了进一步研究这一现象,Paton对一些结构与地衣状菌素相类拟的化合物进行测试,其中包括两个碳链长度分别是8(C8)和16(C16)的甲基季铵盐类化合物。在C8的测试中,实验动物出现呼吸麻痹,这让Paton注意到甲基季铵盐具有肌松作用。Paton对碳链长度从2(C2)到12(C12)甲基季铵盐类化合物的肌松作用做了进一步的实验研究。Paton的工作引起英国医学研究委员会(Medical Research Council,MRC)的注意。受TEA具有降压作用的影响,MRC更关注甲基季铵盐类化合物的降压作用,并推动该类化合物开展降压方面的临床研究。尽管在麻醉师的帮助下初步验证了两个甲基季铵盐类化合物五甲基季铵盐(Pentamethonium)和六甲基季铵盐(Hexamethonium)具有强大的降压作用,但这种降压作用一度被参与试验的麻醉师眼认为一种不受欢迎甚至可能致命的副作用。随着降压药物越来受到关注,甲基季铵盐类化合物的降压作用也逐渐受到临床重视和接受,六甲基季铵盐甚至被称为“药物交感神经切除术”。该类药物降压作用强,一度广泛使用,由于具有较多的副作用,逐渐被其它药物替代。
1940s未,美国波士顿大学医学院(Boston University School of Medicine)的Edward Freis对戊喹(Pentaquine)和美洲藜芦(Veratrum Viride)的降压疗效做了研究。戊喹是一种抗疟药物,第二次世界大战期间,研究疟疾的研究人员注意到,接受高剂量抗疟疾药物治疗的受试者会现直立性高血压。戊喹尽管能够显著降低血压,但除了直立性高血压的问题之外,在治疗高血压的剂量下易出现毒性反应。美洲藜芦是印第安人使用的一种草药,可用于减慢心率和缓解发热。中毒会导致心动过缓、低血压和呼吸暂停。其治疗高血压的治疗窗窄,并且容易引起恶心、呕吐。
1949年汽巴-嘉基Ciba Geigy公司Franz Gross发现肼屈嗪(Hydralazine)具有降压作用。肼屈嗪为一种含有肼结构的药物,该药物源于1945年Druey开发的含肼取代基的杂环驱虫药物。肼屈嗪能够直接扩张小血管,降低外周血管阻力,从而降低血压。肼屈嗪易引起头痛,并且能够反射引起心脏交感神经兴奋和血浆肾素浓度升,从而导致心悸和水钠潴留,长期使用肼屈嗪还可能引起红斑狼疮和类风湿性关节炎。
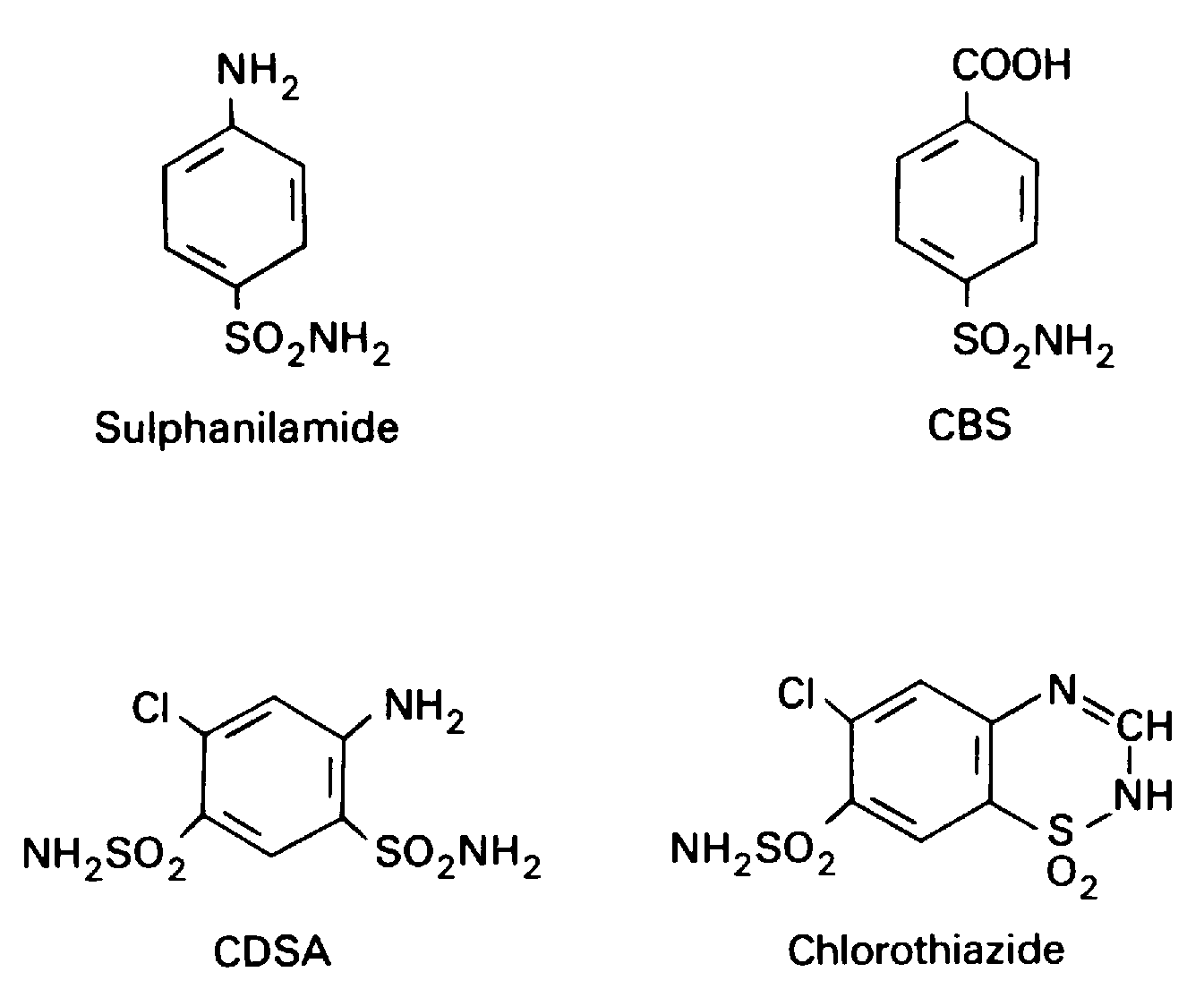
1950s默沙东Merck Sharp & Dohme的Novello和 Sprague合成了一系列含有磺胺(Sulphanilamide)的化合物,以便从中筛选出不引酸中毒的碳酸酐酶抑制剂类利尿剂。Karl Beyer在这些化合物,发现一些化合物如对羧基苯磺胺(CBS)不仅能促进碳酸氢离子的排出,也能促进氯离子的排出,促进碳酸氢离子的排出与抑制碳酸酐酶有关,而促进氯离子排出指向不同的作用靶点。在苯二磺酰胺(Benzenedisulfonamide)引入氯和氨基取代基后,得到的氯二磺胺甲基苯胺(Chlorodisulfamoylaniline,CDSA),其抑制碳糖酐酶的活性显著降低,主要表现为促进氯离子排出,氯离子和钠子的几乎等量排出。通过将CDSA上的氨基和一个磺胺基环化,得到利尿作用更强的氯噻嗪(Chlorothiazide)。1956年底至1957年氯噻嗪选择水肿患者进行早期临床试验,除了利尿改善水肿之外,氯噻嗪显现出良好的降低血压作用,1958年选择高血压患者进行的临床试验进一步验证了氯噻嗪的降压作用。1959年在氯噻嗪的基础上开发出利作用更强的氢氯噻嗪。目前氢氯噻嗪已经成为广泛使用的噻嗪类利尿剂。噻嗪类利尿剂通过作用髓袢升支皮质段和远曲小管前段抑制钠和氯离子的重吸收发挥利尿作用,长期使用,由于钠钾交换作用,也会造成钾离子的丢失。该类药物的降压作用,早期主要依赖于减少血容量,长期降压作用与降低血管阻力有关。
1951年,在美国华盛顿大学(University of Washington)Eugene Roberts的建议下默克Merck公司发现α-甲基谷氨酸(α-Methylglutamic acid)能够抑制谷氨酸脱羧酶。与此同时美国哥伦比亚大学(Columbia University)的Marcel Goldenberg建议Merck通过合成多巴的类似物抑制儿茶酚胺在脱羧酶阶段的生物合成来开发抗高血压药物。Stein合成了一系列多巴的类似物其中包括α-甲基-多巴(α-Methyl-dopa)。由于脱羧酶不是儿茶酚胺体内合成的限速酶,Goldenberg通过动物体内测试,未能发现甲基多巴对脱羧酶有抑制作用,甲基多巴一度被认为不具有生物效应。直到1954年Merck的Sourkes通过体外测试才表明甲基多巴能够抑制对多巴脱羧酶。尽管如此,Merck只是把甲基多巴作为一种供科研使用的普通试剂。1957年德国海德堡大学(University of Heidelberg)的Dengler和Reichel发现甲基多巴能够抑制多巴引起的升压效应。1959年,在缺乏足够的动物实验支持甲基多巴有望成为降压药物的情况下,美国国立心脏研究所(National Heart Institute)的Oates等人开展了甲基多巴临床试验。甲基多巴在人体上表现出非常显著的降压作用。1962甲基多巴首先于英国上市,1963年于美国上市。与同时代的降压药物相比,甲基多巴的副作用相对较少,一度获得广泛使用,目前主要用于妊娠高血压。关于甲基多巴作用机制,在美国国立心脏研究所的研究人员在发型甲基多巴具有降压作用之后不久,他就排除了降压作用与抑制脱羧酶有关,并发现降压与由其活性代谢产物作用于中枢受体有关——脱羧后代谢产物甲基去甲肾上腺素激动中枢肾上腺素α2受体,通过负反馈调节机制,抑制去甲肾上腺释放发挥降压作用。
1957年Kagawa等人在盐皮质激素脱氧皮质酮(Desoxycorticosterone,DOC)的基础上开发出结构与DOC相似,但能够拮抗醛固酮和DOC利钠排钾作用的盐皮质激素拮抗剂螺内酯(Spironolactone)。螺内酯一度成为高血压领域的研究热点。但随着同期肾素-血管紧张素系统被阐明,螺内酯在高血压治疗领域的地位逐渐下降。目前盐皮质激素受体拮抗剂主要用于在难治性高血压。
1958年汽巴Ciba公司Maxwell等人偶然发现发编号为Su-4029的化合物能够阻断苯丙氨(Amphetamine)的升压作用,尽管动物试验显示Su-4029降压作用强并持久的,但临床试验的结果却另人失望。经过进一步筛选,1959年在Su-4029的结构相似的化合物中,筛选出胍乙啶(Guanethidine)。胍乙啶降压作用强并持久,与神经节阻断剂相比,胍乙啶不阻断副感神经,副作用更少。胍乙啶的作用机制与利血平相类似,都通过耗竭交感神经突触前膜囊泡内的去甲肾上腺素,减少去甲肾上腺素释放发挥降压作用。
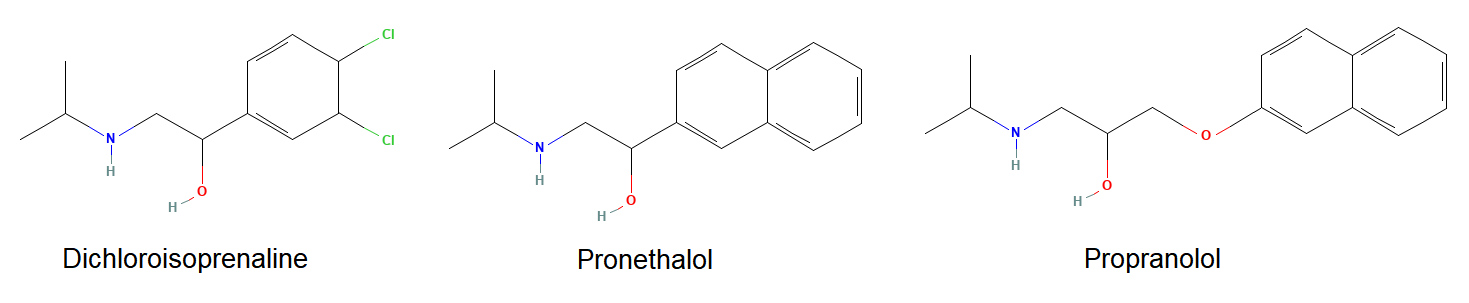
1958年Powell和Slater发现二氯异丙肾上腺素(Dichloroisoprenaline)能够部分阻断肾上腺素的生理效应,造成血压短暂下降。这引起英国帝国化学工业(Imperial Chemicals Industries,ICI)James Black的关注。受Raymond Ahiquist在1948年提出肾上腺素受体可以分为α和β两种亚型假设的影响,James Black相信可以通过阻断β受体减慢心率降低心肌耗氧量的方法来治疗心绞痛。Black测试后显示二氯异丙肾上腺素属于β受体的部分激动剂。Black在ICI合成的二氯异丙肾结构类似物中筛选得到丙萘洛尔(Pronethalol,开发编号ICI 38,174)。丙萘洛尔拮抗心脏肾β上腺素受体,不拮抗外周α受体,初步临床研究显示丙萘洛尔可以降低心绞痛患者的心率,并能够增加运动耐量。由于动物实验显示丙萘洛尔具有致癌性,丙萘洛尔未能实现广泛使用,在丙萘洛尔的基础上,ICI合成出与丙萘洛尔作用相似,无致癌作用的普萘洛尔(Propranolol,开发编号ICI 45,520)。尽管普萘洛尔等非选择性β受体拮抗剂及之后的选择性β1受体拮抗剂已成为心绞痛治疗的基石,但在高血压领域,由于减慢心率的副作用,β受体拮抗剂的治疗地位不如目前常用的其它类型抗高血压药物。
1960年德国Hoechst公司开发出一种能够舒张冠状动脉缓解心绞痛的药物普尼拉明(Prenylamine)。与硝酸酯类抗心绞痛药物不同,普尼拉明具有负性心力的副作用。 1962年德国Knoll公司开发出另一个与普尼拉明作用特点相似但作用更强的药物维拉帕米(Verapamil)。与普尼拉明是苯丙胺(Amphetamine)的结构类似物不同,维拉帕米是罂粟碱(Papaverine)的结构类似物。由于负性心率作用,普尼拉明和维拉帕米一度被认为是β受体拮抗剂。1963年Hoechst和Knoll把普尼拉明与维拉帕米提供给德国弗莱堡大学(University of Freiburg)的Albrecht Fleckenstein,以弄清作用机制。1964年发现普尼拉明与维拉帕米对心肌的作用,与钙离子缺乏引起的效应相似。1967年 Fleckenstein证实普尼拉明与维拉帕米通过拮抗钙离子发挥作用。1968年Knoll公司的席化学家 Ferdinand Dengel提供给Fleckenstein一种维拉帕米的甲氧基衍生物加洛帕米(Gallopamil),Fleckenstein确定Gallopamil是一种作用作用更强的钙拮抗剂。1969年德国Bayer公司的Kroneberg把新开发的含二氢吡啶结构的化合物硝苯地平提供给Fleckenstein以弄清硝苯地平负性肌力和扩张冠脉的作用机制。Fleckenstein测试后显示硝苯地平也是通过拮抗钙离子发挥作用。1969年Fleckenstein证实钙离子拮抗剂通过阻止钙离子跨膜内流发挥作用,既钙离子拮抗剂。二氢吡啶类钙离子拮抗剂与非二氢吡啶类钙离子拮抗剂相比对于血管的选择性更强,并且负性肌力作用,会被扩张血管引起的交感神经活性反射性增高所抵消,目前已成为最常用的抗高血压药物。
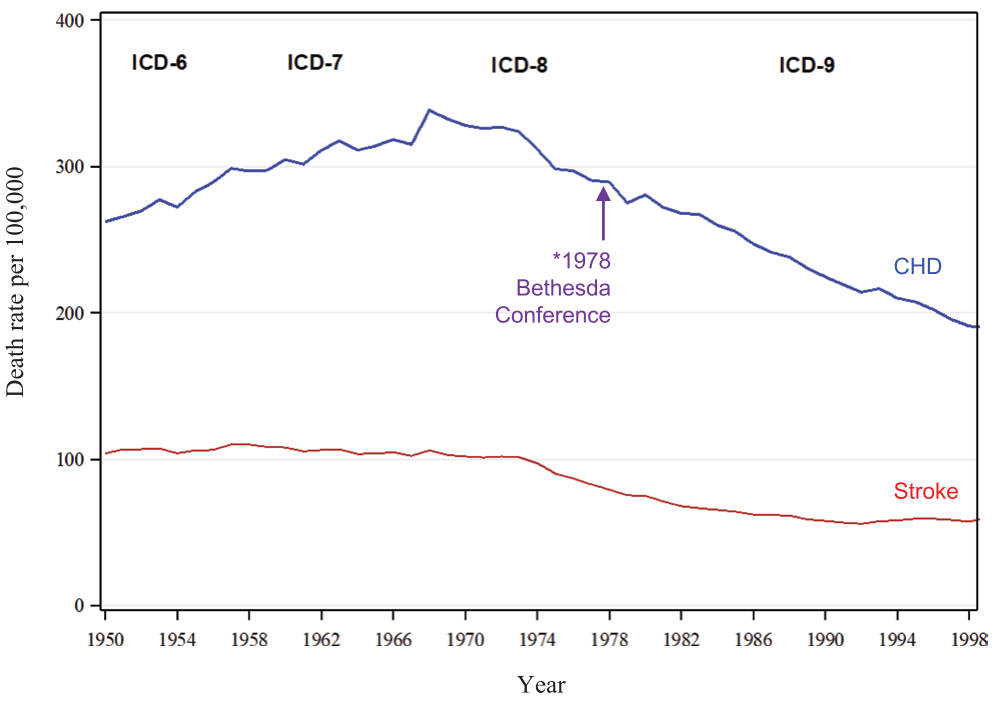
抗高血压药物不断出现,推动高血压管理理念发生转变。1964年《JAMA》发表了Edward Freis组织的美国退伍军人管理局合作研究结果,为长期管理血压,提供了里程碑式的试验证据。美国退伍军人试验显示中高度高血压患者积极使用降压药物治疗,可降低2年内中风、主动脉夹层和恶性高血压的发生率。1969年《Diseases of the Chest》发表了美国公共卫生署(USPHS)国立心脏研究所于1949年启动,关于高血压长期影响的Framingham试验结果。Framingham试验显示轻度血压升高与中重血压升高具有类似的危害性。1970年《JAMA》发表了美国退伍军人试验关于轻度高血压管理的试验结果,证实轻度高血压使用降压药同样也能降低心血管疾病的发生风险。高血压管理理念的改变,扭转了在1967年之前美国心血管疾病的死亡率逐渐上升的趋势,美国于1967迎来心血管疾病死亡率下降拐点。在药物研发方面,降压强度不再是降压药物开发追求的主要目的,能够实现更好管理血压,成为药物筛选的目标。
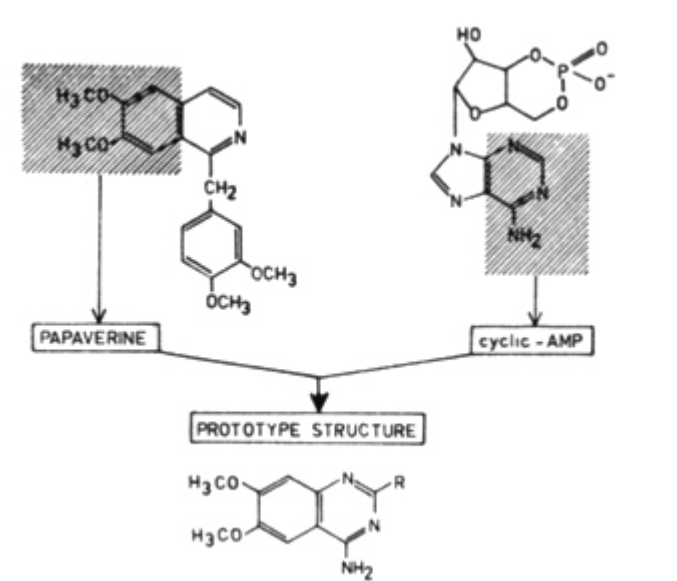
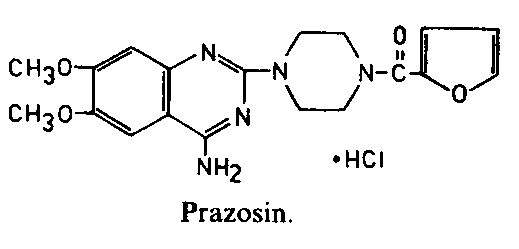
1970s辉瑞Pfizer的研发人员选择在罂粟碱(Papaverine)的基础上开发降压药物。罂粟碱(Papaverine)是一种磷酸二酯酶抑制剂,可以松弛血管和内脏平滑肌,大量时可引起低血压和心动过带。他们通过结合在罂粟碱和环磷酸腺苷(cAMP)的结构,并进行修饰筛选,得到哌唑嗪(Prazosin)。实验显示哌唑嗪不属于磷酸二酯酶抑制剂,而是通过拮抗α受体发挥作用。但哌唑嗪与传统的α受体拮抗剂酚妥拉明(Phentolamine)和酚苄明(Phenoxybenzamine)不同,哌唑嗪扩张血管降低血压,但并不引起心动过速和心收缩加强。1977年辉瑞的Cambridge证实哌唑嗪仅拮抗神经突触后的α受体(α1受体),由于不拮抗突触前膜α受体(α2受体),因此不会通过神经突触前膜的负反馈机制兴奋心脏。由于该类药物易引起体位性低血压,目前已不作为为高血压治疗的首选药物,主要用于高血压伴前列腺增生患者。
70年代未从巴西具窍蝮蛇(Bothrops jararaca)中分离出的含9肽的毒素Teprotide(SQ20881)。巴西科学家Sergio Ferreira发现Teprotide 能够抑制激肽酶。激肽酶分两种亚型激肽酶Ⅰ和激肽酶Ⅱ,后续的研究证实激肽酶Ⅱ与血管紧张素转换酶(ACE)是同一种物质。Teprotide由于不能口服,对高血压和心衰的治疗意义有限。1977年Squibb施贵宝的 Rubin和Cushman在羧肽酶A抑制剂结构基础上开发出非肽ACEI(血管紧张素转换酶抑制剂)类药物卡托普利(Captopril),1978年默克(Merck)实验室合成出不含巯基(-SH)结构的依那普利(Enalapril)。1986年 DuPont杜邦公司研发人员在武田(Takeda)化工的“苗头”化合物S-8307的基础上开发出非肽ARB(血管紧张素Ⅱ受体拮抗剂)类药物类氯沙坦(Losartan)。ACEI和ARB类药物与钙离子拮抗剂相比具有更强的肾保护作用,对心肌也无不良影响,成为目前应用范围最广的抗高血压药物。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3