来源:信达生物 238
2025年9月8日,信达生物宣布替古索司他片用于痛风,中国2期临床试验主要结果发表于2025年亚太风湿病协会联盟大会(APLAR)。

该研究为随机、开放、多中心、平行、活性对照的2期临床研究。共入组84例痛风患者。随机接受替古索司他片50 mg、100 mg、200 mg或非布司他片40 mg治疗。
至第16周,替古索司他50 mg、100 mg和200 mg组血尿酸达到<360μmol/L(6mg/dL)的比例均显著高于非布司他40 mg组。替古索司他50 mg、100 mg、200 mg和非布司他40 mg组血尿酸达到<360μmol/L的比例分别为55.0%、81.0%、85.7%和18.2%。相对于非布司他组,替古索司他50 mg、100 mg、200 mg组血尿酸达到<360 μmol/L的比例分别为36.8%(9.7至63.9,P=0.008)、62.8%(39.5至86.0,P<0.001)和67.5%(45.至89.5,P<0.001)。
替古索司他50 mg、100 mg、200 mg和非布司他40 mg组血尿酸达到<300 μmol/L(5 mg/dL)的的比例分别为30.0%、61.9%、81.0%和9.1%。相对于非布司他组,替古索司他50 mg、100 mg、200 mg组血尿酸达到<360 μmol/L的比例分别为20.9%(-2.5至44.3,P=0.046)、52.8%(28.8至76.8,P<0.001)和71.9%(51.2至 92.5P<0.001)。替古索司他50 mg、100 mg、200 mg和非布司他40 mg组血尿酸相对于基线分别变化-38.66%、-48.61%、-57.11%和-24.11%。在安全性方面,替古索司他与非布司他不良事件的发生率相似,均为轻至中度。在痛风急性发作方面,替古索司他与非布司他相似,主要发生在给药后前4周。
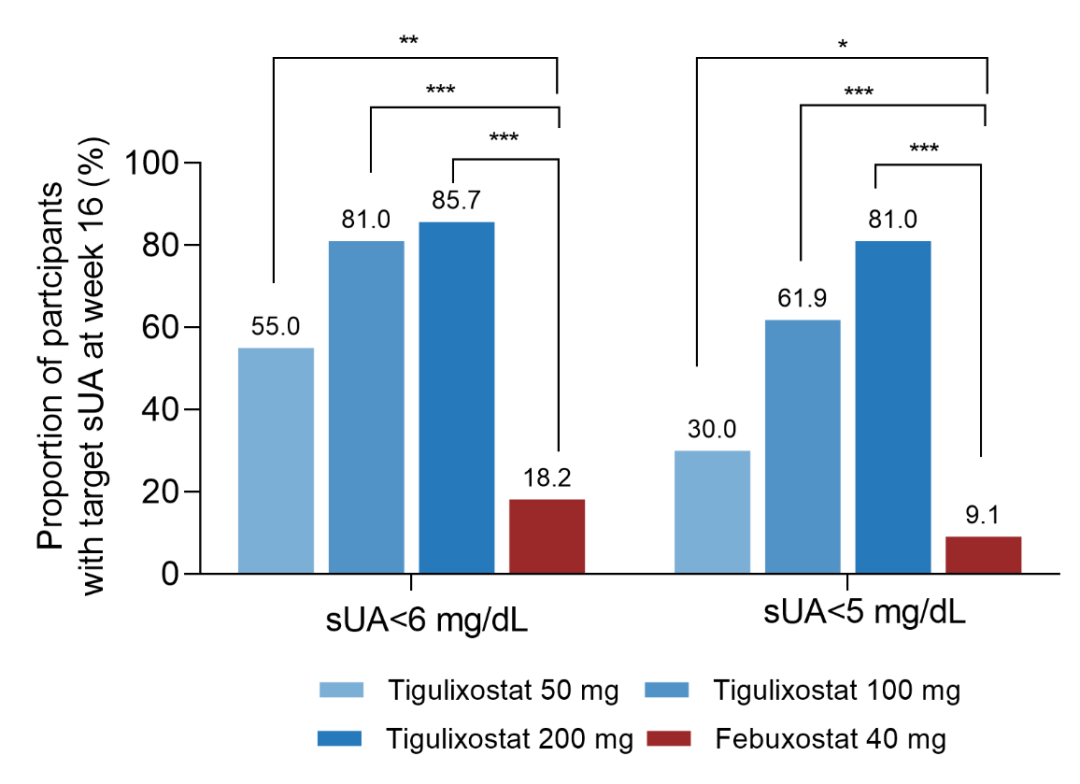
* P<0.05,** P<0.01, *** P<0.001
替古索司他(Tigulixostat)由LG开发(LG研发代号: LC350189),与非布司他均属于黄嘌呤氧化酶(XO)抑制剂类药物。通过抑制黄嘌呤氧化酶活性,阻止次黄嘌呤和黄嘌呤代谢为尿酸,从而减少尿酸生成。2022年信达生物以1,000万美金首付款,总额不超过8,550万美金潜在里程碑付款,及中国地区年度净销售额梯度特许使用费的形式,获得替古索司他在国的独家开发和商业化权利(信达生物研发代号: IBI350)。
尽管替古索司他与非布司他在抑制黄嘌呤氧化酶的活性相当(Seonghae Yoon., 2015),但在本次2期试验中,替古索司他相较非布司他,展现出更显著的降尿酸效果。

免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
|
推荐阅读: ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
关注“药研苑”公众号,及时掌握最新的药物研发动态。
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2025年9月8日,信达生物宣布替古索司他片用于痛风,中国2期临床试验主要结果发表于2025年亚太风湿病协会联盟大会(APLAR)。
发布日期:2025-09-08 浏览数:237
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3