来源:赛诺菲 1221
2025年9月4日,赛诺菲Sanofi宣布其靶点OX40L单克隆抗体Amlitelimab用于特应性皮炎(AD)的成人和青少年3期临床试验COAST 1达到所有主要和关键次要终点。

COAST 1是一项全球多中心、随机、双盲、平行安慰剂对照、3臂3期临床试验。共纳入601名12岁及以上中重度特应性皮炎成人及青少年患者。入组患者患者随机接受Amlitelimab 每4周1次、每12周1次或安慰剂治疗。Amlitelimab组负荷量为500mg(体重<40 kg者负荷剂量为250mg),治疗剂量为250 mg(体重<40 kg者治疗量为125mg)。
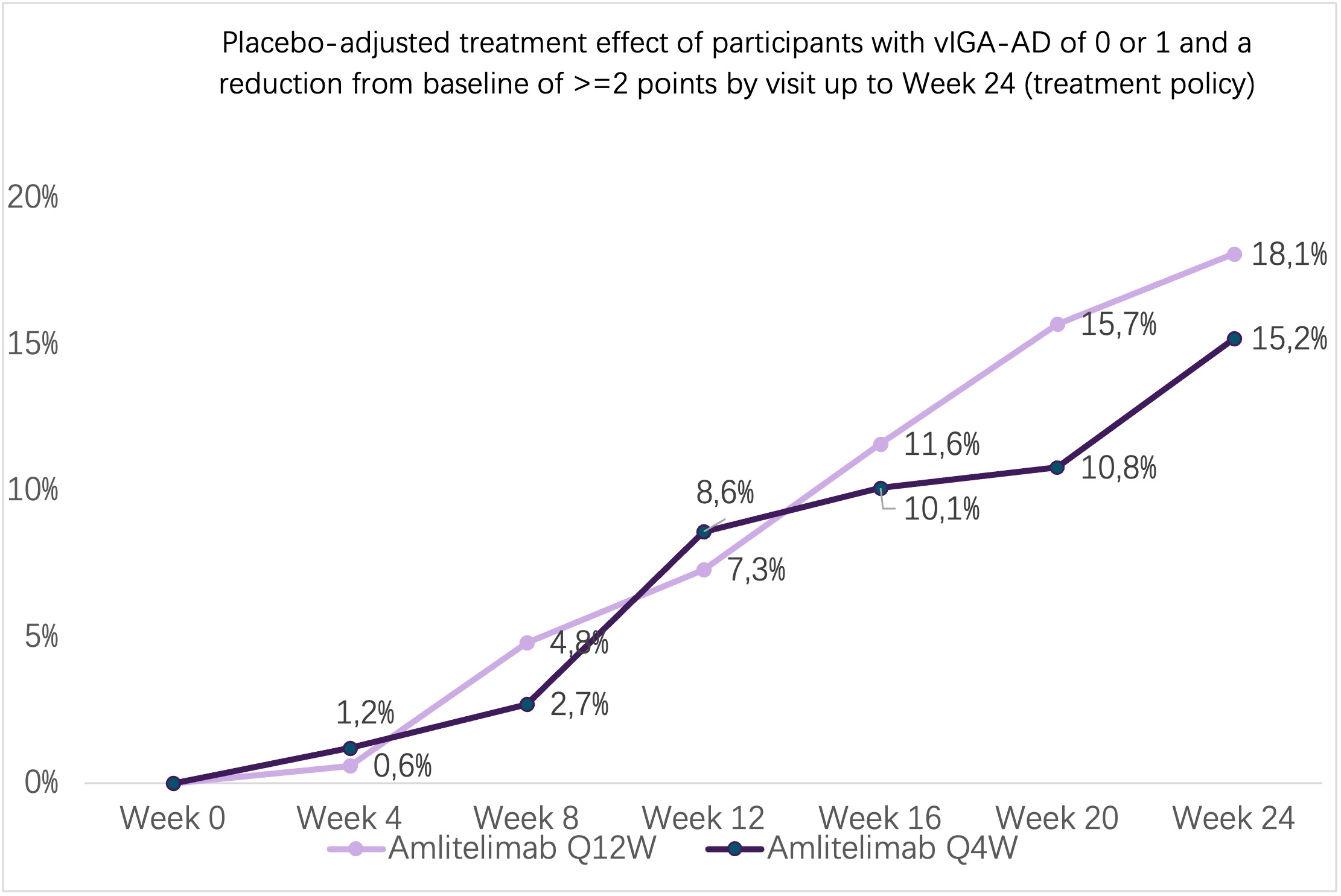
至第24周Amlitelimab每4周1次组、每12周1次组及安慰剂组《研究者AD整体评估验证量表(vIGA-AD)》评分为0分(清洁)或1分(几乎清洁)的比例分别为21.1%(p <0.01)、22.5%(p <0.01)和9.2%。达到《湿疹面积和严重程度指数改善≥75%(EASI-75)》的比例分别为35.9%(p <0.001)、39.1%(p <0.001)和19.1%。两个治疗组,在治疗期间疗效逐渐增加,没有观察到平台期。
最常见(任何剂量组为≥5%)的治疗期间不良事件(TEAE)包括特应性皮炎、鼻咽炎和上呼吸道感染。与Amlitelimab治疗组相比,安慰剂组更常见。与安慰剂相比Amlitelimab组注射部位反应的发生率更高(Amlitelimab组2.2%,安慰剂组0.7%)。发热(Amlitelimab组为1.1%,安慰剂组为0.7%)和寒战(Amlitelimab组为0.4%,安慰剂组为0%)发生率较低。
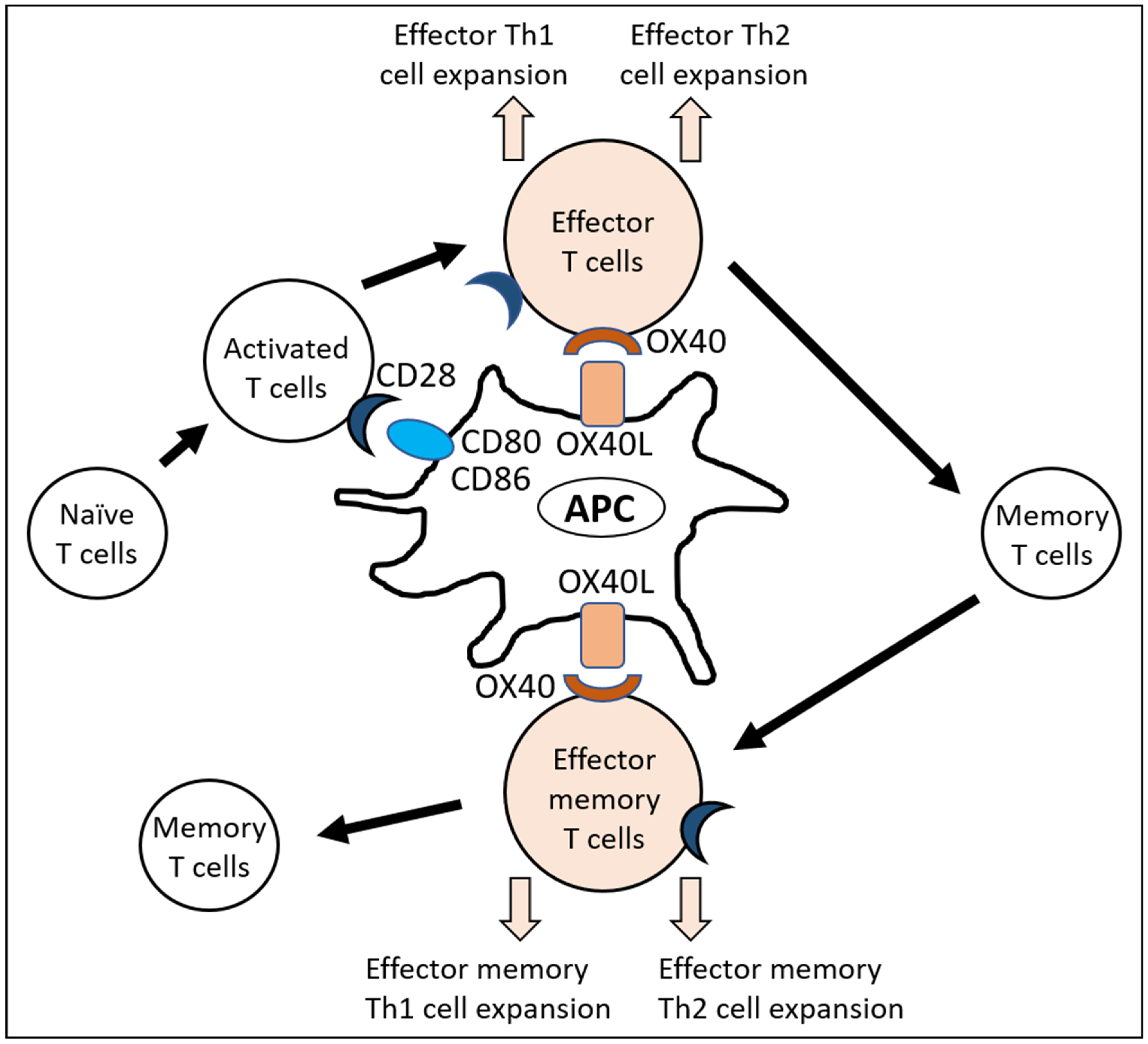
Amlitelimab(研发代号SAR445229、KY1005)为全人源抗OX40L单克隆抗体。OX40L为OX40的配体,OX40L主要在抗原呈递细胞上表达,OX40在效应和调节性T细胞上表达。OX40L作用于OX40,能够增强T细胞的促炎症反应。Amlitelimab与OX40L结合,不耗竭T细胞,但能够阻断OX40L作用于OX40,发挥抗炎作用。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

2025年9月4日,赛诺菲Sanofi宣布其靶点OX40L单克隆抗体Amlitelimab用于特应性皮炎(AD)的成人和青少年3期临床试验COAST 1达到所有主要和关键次要终点。
发布日期:2025-09-04 浏览数:1220

2024年12月13日,爱科诺生物宣布其RIPK2 抑制剂AC-101治疗溃疡性结肠炎(UC)2期临床试验的IND申请已获得美国FDA批准。
发布日期:2024-12-13 浏览数:1099

2025年3月2日,罗氏Roche公布了奥马珠单抗用于儿童和成人食物过敏3期临床试验OUtMATCH研究第2阶段和第3阶段的的研究数据。
发布日期:2025-03-02 浏览数:1068

2025年4月9日,荣昌生物宣布在美国神经病学学会(AAN)年会期间,以口头报道形式发布泰它西普用于全身型重症肌无力(gMG)3期临床试验的研究结果。
发布日期:2025-04-09 浏览数:943
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3