
乌帕替尼属于JAK1的选择性抑制剂,对于JAK1的选择性远高于JAK2、JAK3和TYK2。因此避免抑制JAK2产生的不良反应。
结构:
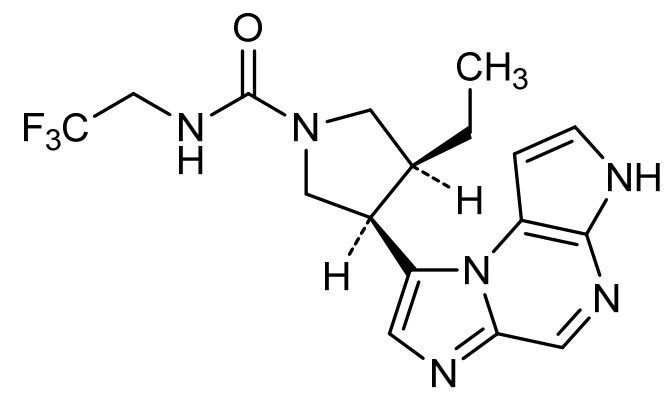
介绍:
乌帕替尼(Upadacitinib),商品名瑞福(RINVOQ),研发编号ABT-494是由是AbbVie开发的选择性JAK1抑制剂。
乌帕替尼的开发源于考虑将托法替布(Tofacitinib)的吡咯并嘧啶二元环结构与嘧啶氨基上的甲基拼合成三元环,来开发新的JAK抑制剂(Stacy Van Epps., 2013)。
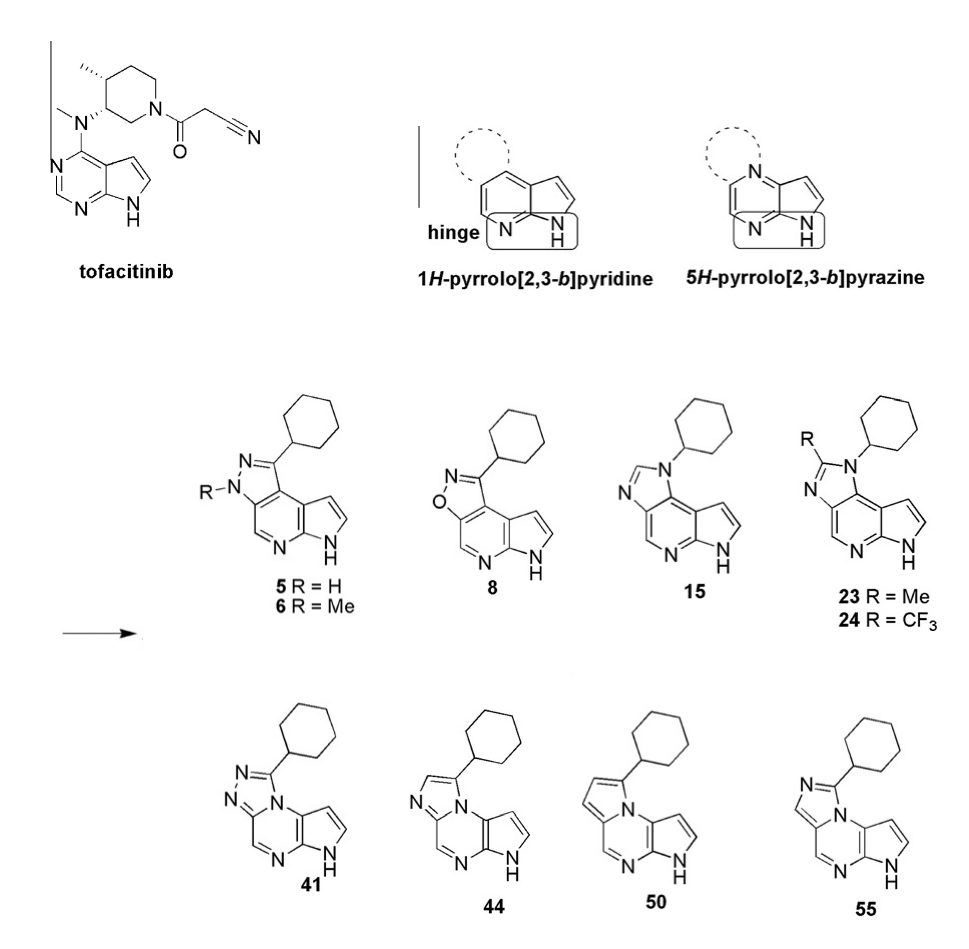
| Compound | Jak 1 enzyme (μM) | Jak 1 cellb (μM) | Jak 2 cell (μM) | Jak2/Jak1 Cellular selectivity |
| 5 | 0.003 | 0.17 | 4.2 | 25x |
| 6 | 0.09 | 1.2 | 0.89 | 1x |
| 8 | 0.02 | 0.43 | 1.6 | 4x |
| 15 | 0.03 | 0.21 | 9.8 | 47x |
| 23 | 0.02 | 0.18 | 6.6 | 37x |
| 24 | 0.04 | 0.97 | >20 | 21x |
| 41 | 0.03 | 0.35 | 15.8 | 45x |
| 44 | 0.004 | 0.15 | 4.8 | 32x |
| 50 | 0.02 | na | >20 | na |
| 55 | 0.01 | 0.37 | 2.8 | 8x |
通过对比托法替布和JAK1及JAK2形成复合物晶体结构,可以看到在托法替布氰基一端与JAK内一个富含甘氨酸(Glycine)残基的环相结合。由于该环末端存在His885(JAK1)/Asn859(JAK2)残基上的差异,导致JAK1由于His885与Asp1003之间的作用,使得该富含甘氨酸残环更加封闭。造成JAK1和JAK2结构上存在差异。
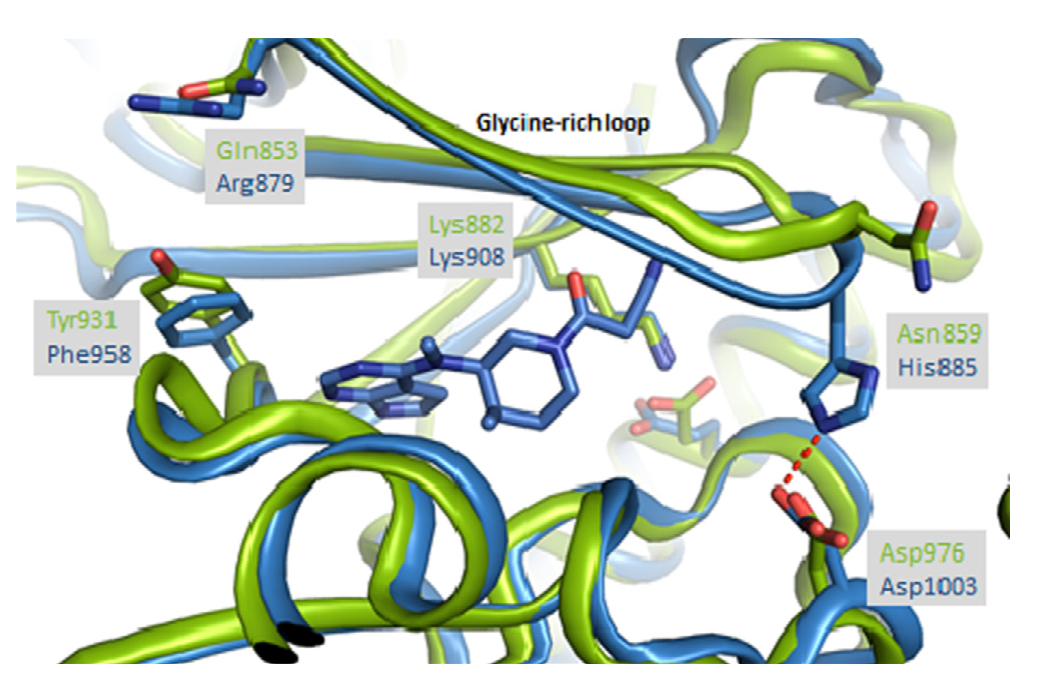
在44的基础上通过结合改变托法替布氰基端的结构,并优化后,得到乌帕替尼(Upadacitinib)。乌帕替尼对于JAK1的选择性远高于JAK2、JAK3和TYK2。因此避免抑制JAK2产生的不良反应。
| Recombinant Human Kinase | IC50 nM | Fold selectivity vs. JAK1 |
| in Biochemical Assays | ||
| JAK1 | 47 +/− 6.1 | 1 |
| JAK2 | 120 +/− 29.6 | 2.5 |
| JAK3 | 2304 +/− 380.3 | 49 |
| TYK2 | 4690 | 100 |
| Engineered Cellular Assays | ||
| Ba/F3 Cellular | IC50 nM | Fold selectivity vs. JAK1 |
| JAK1 | 14 | 1 |
| JAK2 | 593 +/− 118.7 | 42 |
| JAK3 | 1860 +/−207.2 | 133 |
| TYK2 | 2715 +/− 548.7 | 194 |
2018年,Gerd R Burmester等人发表乌帕替尼治疗类风湿性关节炎的3期临床试验SELECT-NEXT结果。共纳入661名传统常改善病情抗风湿药物(DMARD),包括甲氨蝶呤、柳氮磺吡啶或来氟米特,治疗不佳的患者,按1:1:1比例接受乌帕替尼30mg缓释制剂、15mg缓释制剂或安慰剂治疗12周,12周后安慰剂组随机接受乌帕替尼30mg缓释制剂、15mg缓释制剂继续治疗。在第12周,乌帕替尼15 mg剂量组221例患者中有141例(64%; 95% CI 58-70)符合美国风湿病协会(ACR)活动期类风湿关节炎缓解达到20%标准(ACR20),乌帕替尼30mg剂量组219例患者中有145例(66%; 60-73)达到ACR20,安慰剂组221例患者中有79例(36%; 29-42)达到ACR20。与安慰剂相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。乌帕替尼15 mg、30m和安慰剂组达到类风湿 DAS28评分标准C反应蛋白(CRP)≤3.2的患者数分别为107例(48%; 95% CI 42–55)、105例(48%; 41–55)和 38 例(17%; 12–22)。与安慰剂相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。乌帕替尼15 mg、30m和安慰剂组分别有125 例(57%)、118 例 (54%)、108 例(49%) 报告发生不良事件。≥5%的不良事件包括恶心(乌帕替尼15 mg、30m和安慰剂组分别有16例7%、3例1%、7例3%)、鼻咽炎(12例5%、13例6%、9例4%)、上呼吸道感染(12例5%、12例5%、9例4%)、头痛(9例4%、7例3%、12例5%)。乌帕替尼15 mg、30m和安慰剂组分别有 64 例(29%)、 69例(32%) 、47例(21%)报告出现其它感染。有3例患者出现带状疱疹感染(安慰剂组1例[<1%、。乌帕替尼15 mg组1例<1%、乌帕替尼30mg组1例[<1%)、1例原发性水痘带状疱疹病毒感染(乌帕替尼30mg组1例<1%)、2例恶性肿瘤(均在乌帕替尼30mg组)、 1例严重不良心血管事件(乌帕替尼30mg组)和5例严重感染(安慰剂组1例<1%、乌帕替尼15 mg组1例<1%、乌帕替尼15 mg组3例1%)。试验期间没有死亡病例报告(Gerd R Burmester.,2018)。
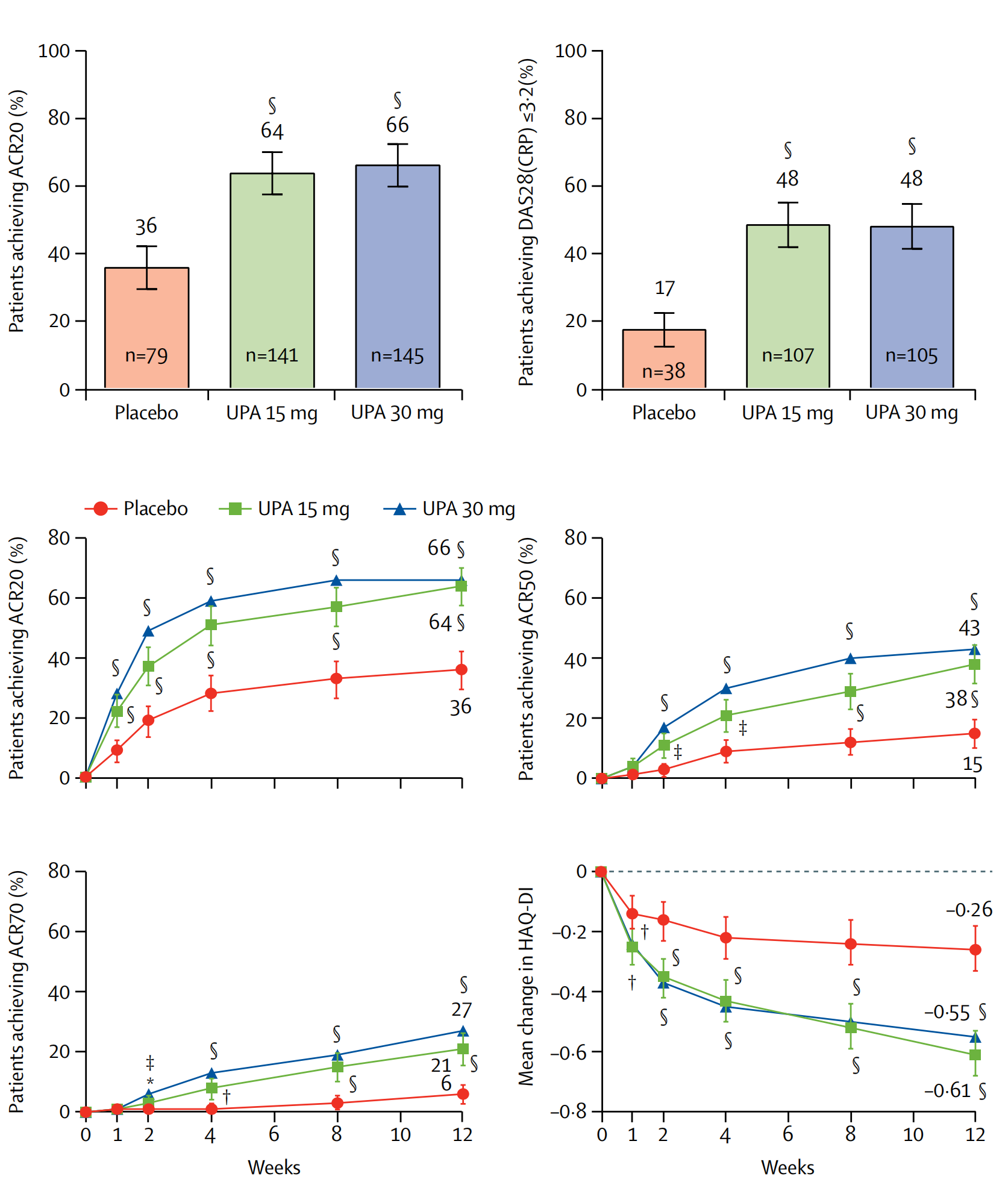
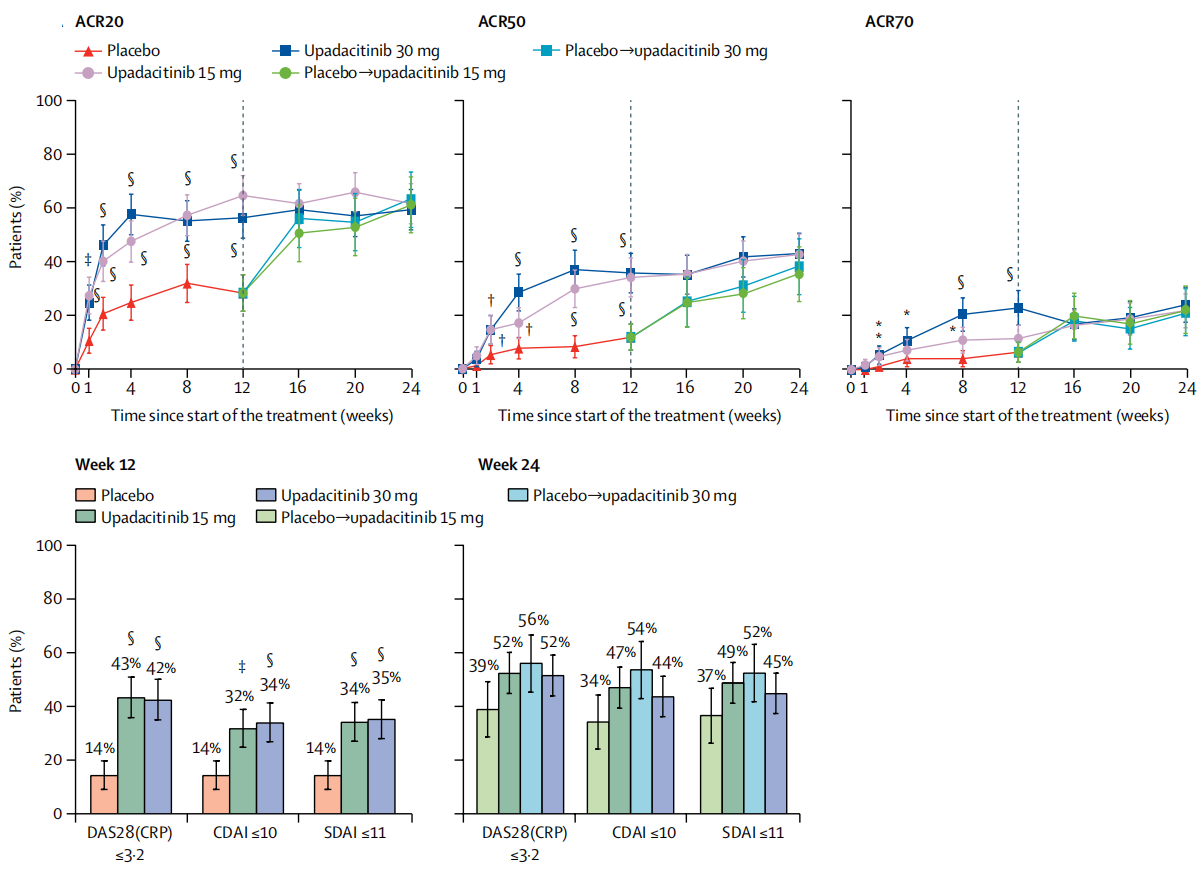
2018年,Mark C Genovese等人发表乌帕替尼治疗类风湿性关节炎的3期临床试验ELECT-BEYOND结果。共纳入499 名传统常改善病情抗风湿药物(DMARD)治疗不佳的患者,在继续使用原有DMARD的基础上,按1:1:1比例接受乌帕替尼30mg缓释制剂、15mg缓释制剂或安慰剂治疗12周,12周后安慰剂组随机接受乌帕替尼30mg缓释制剂、15mg缓释制剂继续治疗。,在第12周,乌帕替尼15 mg剂量组106 例(65%; 95% CI 57-72)达到ACR20,乌帕替尼30mg剂量组 93例(56%; 49-64)达到ACR20,安慰剂组221例患者中有48例(28%; 22-35)达到ACR20。与安慰剂相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。乌帕替尼15 mg、30m和安慰剂组DAS28(CRP)≤3.2的患者数分别为71例(43%; 95% CI 36-51)、70 例(42%; 35-50)和24例(17%; (14%; 9-20)。与安慰剂相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。在12周治疗期间内乌帕替尼15 mg剂量组不良事件发生率为55%与安慰剂组相似(56%),低于乌帕替尼30 mg剂量组(67%)。≥5%的不良事件包括上呼吸道感染(乌帕替尼15 mg、30m和安慰剂组分别有13例8%、10例6%、13例8%)、鼻咽炎(7例4%、9例5%、11例7%)、尿路感染(15例9%、9例5%、10例6%)和类风湿性关节炎恶化(4例2%、6例4%、10例6%)。乌帕替尼30 mg剂量组严重不良事件的发生高于乌帕替尼15 mg剂量组(12例7%和8例5%)。乌帕替尼30 mg剂量与15 mg剂量组及安慰剂组相比发生严重感染、带状疱疹、及由于不良事件停药的比例更高。乌帕替尼组发生1例肺栓塞、3例恶性肿瘤、1例严重不良心血管事件、1例死亡事件(Mark C Genovese., 2018)。
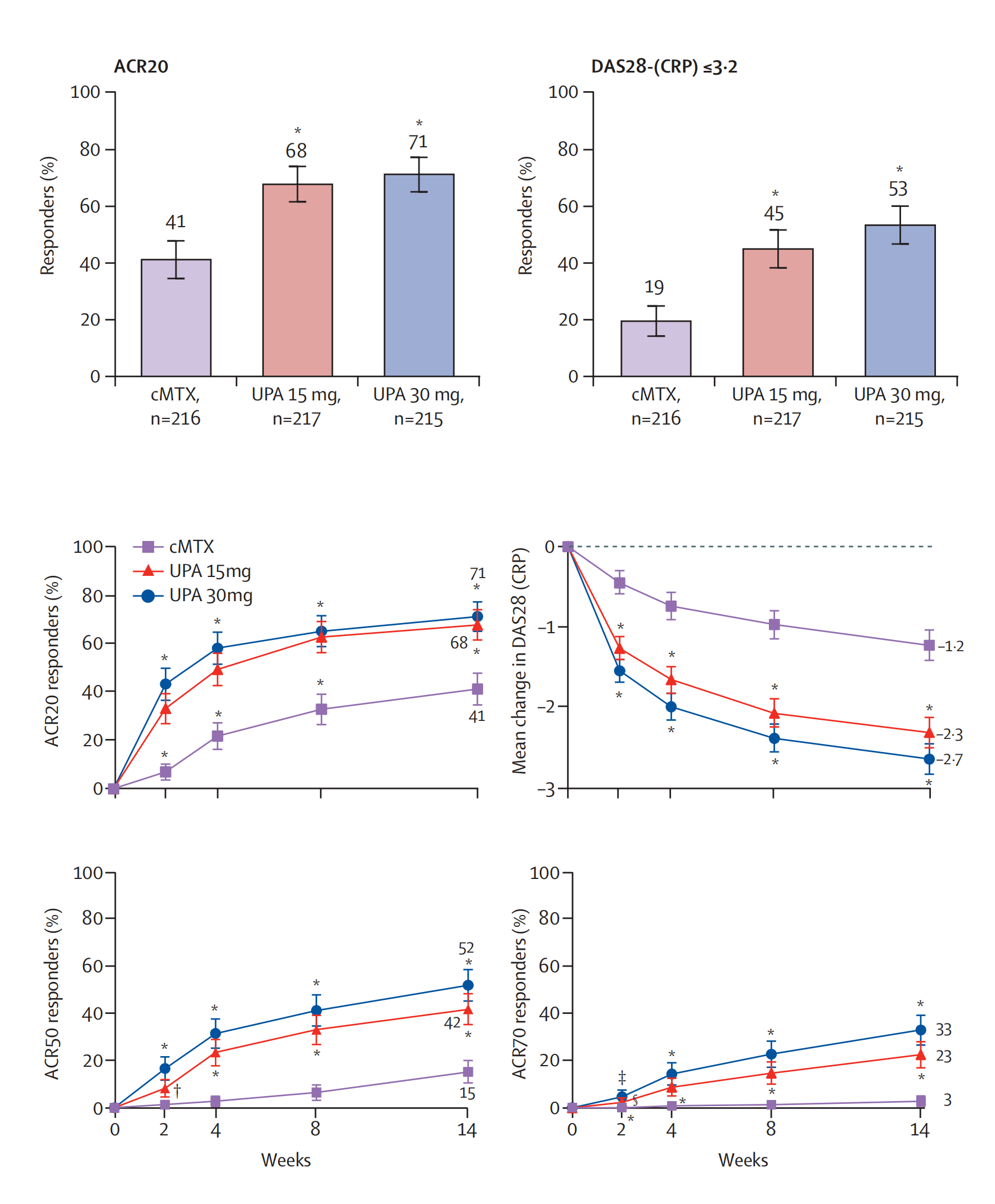
2019年,Josef S Smolen等人发表乌帕替尼治疗类风湿性关节炎的3期临床试验SELECT-MONOTHERAPY结果。共纳入648 名传统常改善病情抗风湿药物(DMARD)甲氨蝶呤治疗不佳的患者,按1:1:1比例接受乌帕替尼30mg、15mg一天或继续使用甲氨蝶呤治疗14周,12周后甲氨蝶呤组转为随机接受乌帕替尼30mg或15mg一天一次继续治疗。在第12周,乌帕替尼15 mg、乌帕替尼30mg剂量组和甲氨蝶呤组分别有147例(68%; 95% CI 62-74)、153例 (71%;65-7)和89例 (41%; 35-48)达到ACR20。与甲氨蝶呤相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。达到DAS28(CRP) ≤3.2的患者数分别为97 例(45%; 95% CI 38-51)、 114例(53%; 46-60)和 42 例(19%; 14-25)。与甲氨蝶呤相比,乌帕替尼30m和15mg剂量组均达到p<0.0001。乌帕替尼15 mg、30m和安慰剂组分别有125 例(47%)、105 例 (49%)、 102例(47%) 报告发生不良事件。甲氨蝶呤组、乌帕替尼15mg和乌帕替尼30m剂量组分别有1例(<1%)、3例(1%)和6例(3%)出现 带状疱疹。甲氨蝶呤组、乌帕替尼15mg分别有1例(<1%)、2例(1%)发生恶性肿瘤。乌帕替尼15mg和乌帕替尼30m剂量组分别有1例(<1%)和2例(1%)发生严重不良心血管事件。乌帕替尼15mg有1例(<1%)发生肺栓塞。乌帕替尼15mg有1例(<1%)死亡病例(出血性血卒中)(Josef S Smolen.,2019)。
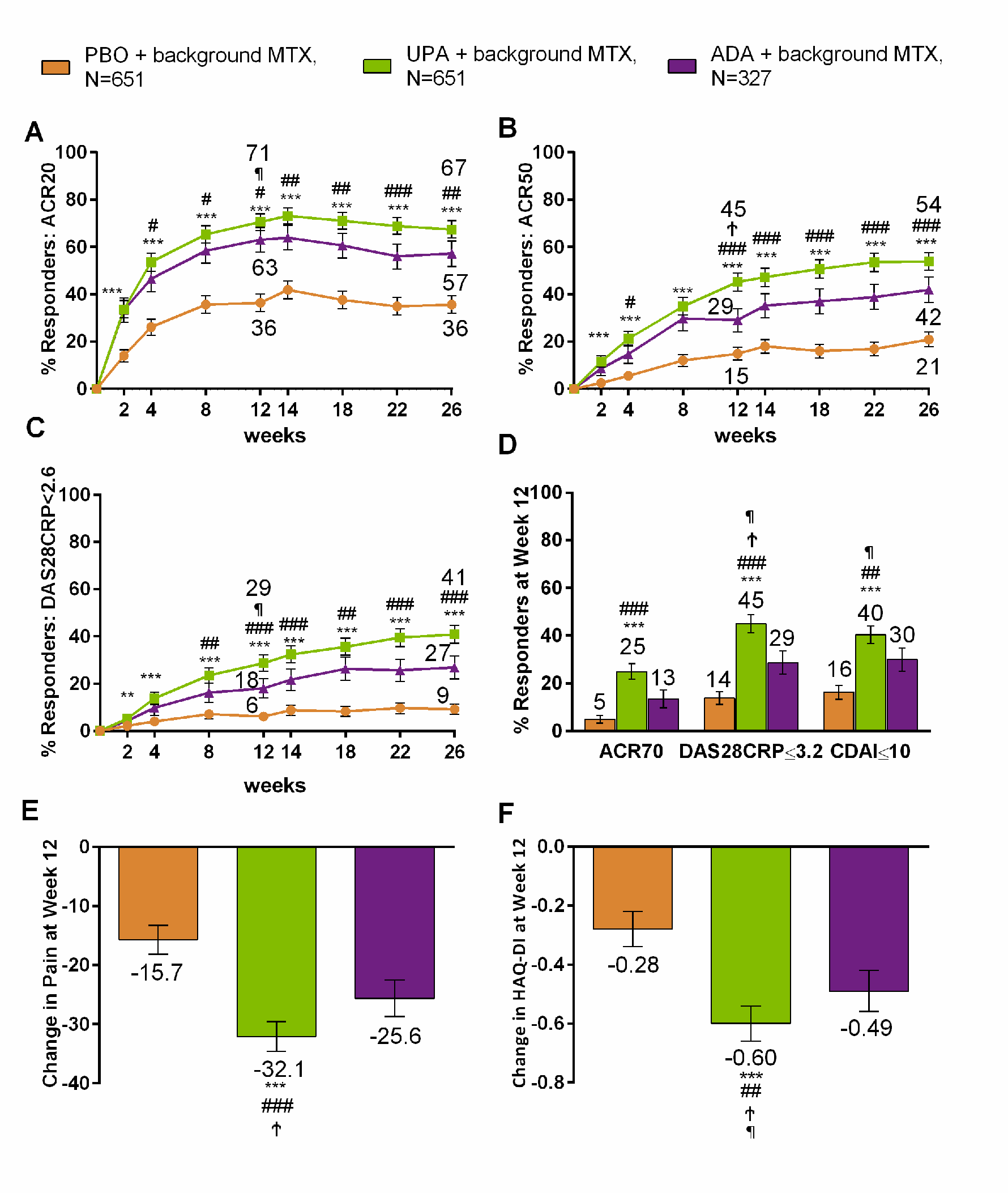
2019年,Roy Fleischmann等人发表乌帕替尼治疗类风湿性关节炎的3期临床试验SELECT-MONOTHERAP结果。共纳入1,629 名传统常改善病情抗风湿药物(DMARD)甲氨蝶呤治疗不佳的患者,按2:2:1比例接受乌帕替尼(15mg/天)、安慰剂或阿达木单抗注(40 mg 每两周)治疗26周,在治疗期间患者继续接受固定剂量的甲氨蝶呤进行治疗。在第12周,乌帕替尼组和安慰剂组达到ACR20的比例分别为71%的和36%(P ≤ 0.001),达到DAS28-CRP<2.6的分别为29%和6%(P ≤ 0.001)。乌帕替尼组达到ACR50、DAS28-CRP≤3.2,改善疼痛严重程度评分、健康评估问卷残疾指数(health assessment questionnaire disability index,HAQ-DI)方面显著优于阿达木单抗组。在第26周达到完全缓解低疾病活动状态的比例乌帕替尼组显示高于安慰剂或阿达木单抗组。影像学进展的比例乌帕替尼显著优于安慰剂组。在26周治疗期间,阿达木单抗组发生严重不良事件及由于生严重不良事件导致停药的比例更高,阿达木单抗组;带状疱疹、肌酸磷酸激酶(CPK)升高的比例更高。共出现3例恶性肿瘤、5例严重不良事件和4例死亡,均不在乌帕替尼组。共报告了 6 例静脉血栓栓塞事件(安慰剂组 1 例乌帕替尼组 2 例,阿达木单抗组 3 例)(Roy Fleischmann., 2019)。
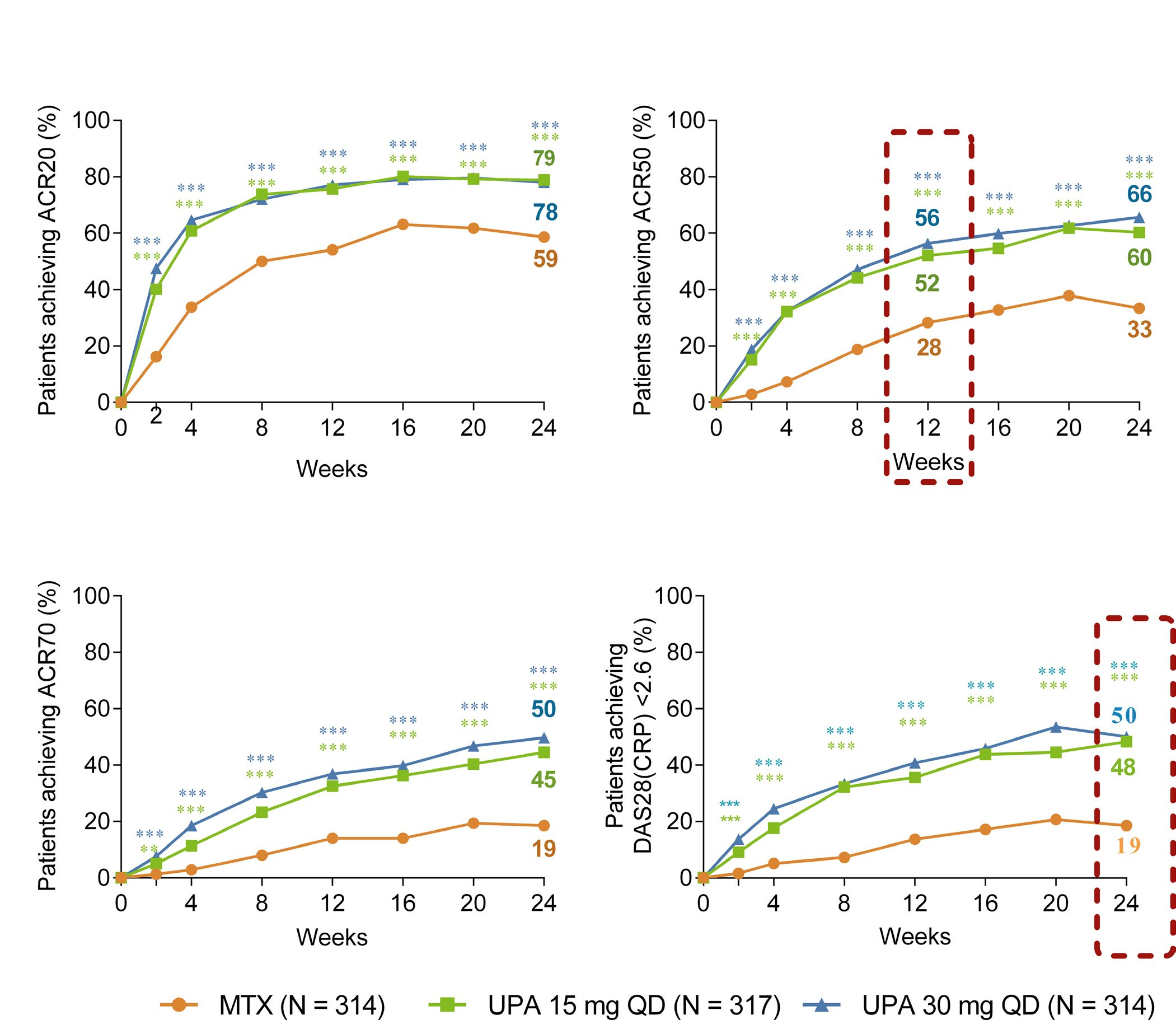
2020年,Ronald van Vollenhove等人发表乌帕替尼治疗早期类风湿性关节炎的3期临床试验SELECT-EARLY结果。共纳入 947名类风湿性关节炎患者,按1:1:1比例接受乌帕替尼30mg、15mg一天一次或甲氨蝶呤(MTX)7.5-20 mg/周治疗24周。乌帕替尼315mg、30mg及MTX组第12周达到ACR50的比例分别为52%、56%和28%(P < 0.001),第24周DAS28-CRP<2.6的比例分别为48%、50%和19%(P < 0.001)。 乌帕替尼315mg、30mg及MTX组没有影像学进展(改良总Shar 评分≤0)的比例分别为 88% 、89% 、50%和78%(P < 0.01)。第24周,MTX组(65%)和 乌帕替尼 15 mg组(64%)不良事件的发生率相似,乌帕替尼30 m组(71%)略高。共6例死亡病例报告(乌帕替尼 15 mg组2例,乌帕替尼 30 mg组3例,MTX组1例)(Ronald van Vollenhove.,2020)。
基于上述5项研究结果,FDA于2019年8月16日批准乌帕替尼用于治疗中重度类风湿性关节炎。
2021年12月14日,FDA基于SELECT-PsA 1和 SELECT-PsA 2两项3期研究结果,批准乌帕替尼用于治疗活动性银屑病关节炎。在 SELECT-PsA 1 和 SELECT-PsA 2 3 期临床试验中,乌帕替尼15mg组达到ACR20的比例分别为71% 和 57%,高于安慰剂组(36%和24%)。
2022年1月14日,FDA批准乌帕替尼治疗成人和12岁及以儿童难治性中重度特应性皮炎。
2022年3月16日,FDA批准乌帕替尼用于治疗成人中度至重度活动性溃疡性结肠炎。
2022年4月29日,FDA 批准乌帕替尼用于治疗成人活动性强直性脊柱炎。
2022年10月21日,FDA 批准乌帕替尼用于治疗活动性非放射性轴性脊椎关节炎。
2023年5月18日,FDA 批准乌帕替尼用于治疗中重度活动性克罗恩病。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3