来源:维立志博 764
2025年8月25日,维立志博宣布其靶向GPRC5D/CD3的双特异性抗体LBL-034,用于多种复发/难治的浆细胞肿瘤2期临试验(CTR20232974),完成首例患者给药。

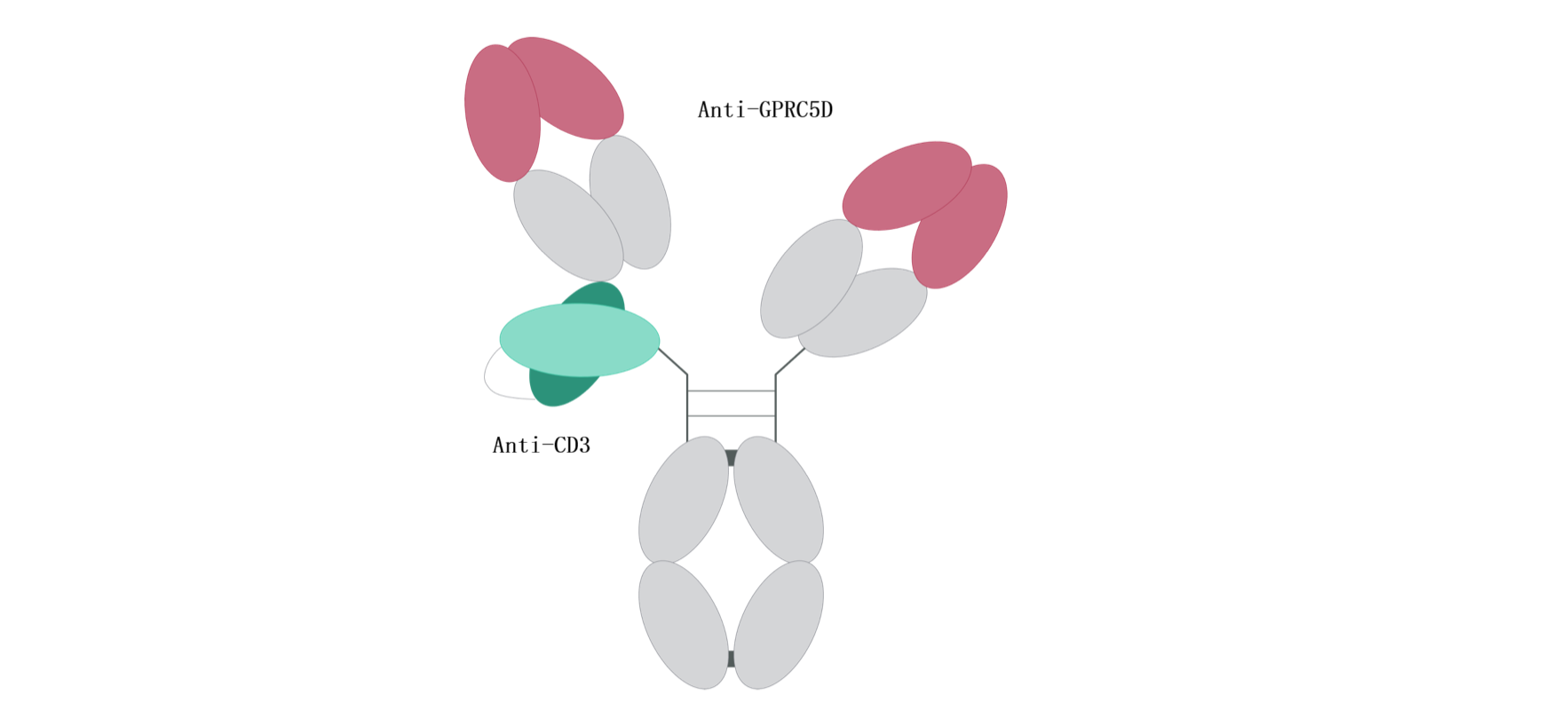
LBL-034为靶向GPRC5D/CD3的T细胞衔接器双特异性抗体。GPRC5D为G蛋白偶联受体在骨髓瘤细胞系中高度表达。CD3为T细胞的共受体,通过与T细胞受体(TCR)结合,参与信号传导。LBL-034一方面与骨髓瘤细胞GPRC5D结合,另一方面与T细胞CD3结合,引导T细胞杀伤骨髓瘤细胞。LBL-034使用非对称2:1结构设计,通过优化与CD3亲和力及空间位阻作用,以降低T细胞非特异性激活风险。
LBL-034用于多发性骨髓瘤 (MM)1期临床试验15例患者研究数据显示,没有发生≥3级的细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)(Ling Qin., 2024)。
目前,仅有强生的GPRC5D/CD3双特异性抗体(塔奎妥单抗Talquetamab)在国内上市。塔奎妥单抗治疗复发或难治性多发性骨髓瘤1/2期临床试验MonumenTAL-1研究显示,GPRC5D/CD3双特异性抗体治疗复发或难治性多发性骨髓瘤(包括继往接受靶向BCMA的T细胞衔接器双特异性抗体或CAR-T治疗)方面,具有积极的治疗意义。如在后续试验中,LBL-034能够被证实疗效不低于塔奎妥单抗,安全性更优,LBL-034将成为塔奎妥单抗强有力的竞争对手。
注:MonumenTAL-1研究共纳入375名复发或难治性多发性骨髓瘤患者。试验结果显示塔奎妥单抗0.4 mg/kg(1周1次)组总缓解率达到74%(106/143,95% CI 66-81),0.8 mg/kg(2周1次)组达到69%(107/154,95% CI 62-77),继往接受T细胞重定向疗法(包括靶向BCMA的T细胞衔接器双特异性抗体或CAR-T)塔奎妥单抗治疗组的总缓解率达到67%(52/78,95% CI 55-77)。上述3组最常见的3-4级不良事件为中性粒细胞减少(44例[31%]、33例[21%]和37例[47%])、贫血(45例[31%]、40例[26%]和21例[27%])和淋巴细胞减少症(37例[26%]、40例[26%]和13例[17%])。共发生12例死亡病例,分别为5例、7例和0例,均认为与治疗无关(Ajai Chari., 2025)。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2024年10月18日,礼新医药其PD-1/VEGF双特异性抗体药LM-299已在中国启动实体瘤1期临床试验。
发布日期:2024-10-18 浏览数:3217

2025年8月8日,荣昌生物宣布其抗PD-1/VEGF双特异性抗体RC148用于晚期恶性实体肿瘤2期临床试验申请,获得美国食品药品监督管理局(FDA)批准。
发布日期:2025-08-08 浏览数:1279

2025年3月4日,基石药业(CStone Pharmaceuticals)宣布CS2009的全球多中心1期临床试验完成首例患者给药,该患者未发生输液反应或其他不良事件。
发布日期:2025-03-04 浏览数:1119

2025年3月10日,辉瑞Pfizer宣布易瑞欧®(埃纳妥单抗)获得国家药品监督管理局附条件批准,用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38单克隆抗体)的复发…
发布日期:2025-03-10 浏览数:1045
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3