来源:强生 285
2025年2月11,强生宣布拓立珂®(塔奎妥单抗注射液)获得国家药品监督管理局批准,单药适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38抗体)的成人复发或难治性多发性骨髓瘤(RRMM)。

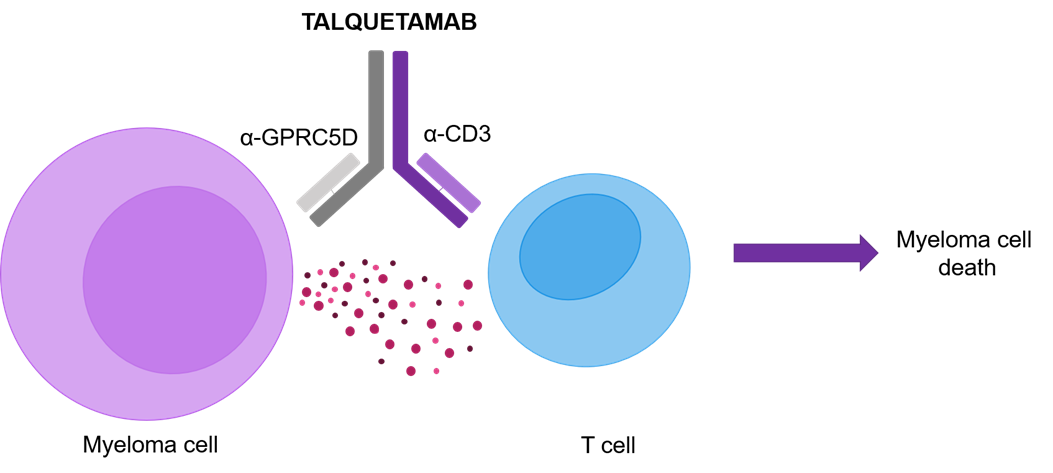
塔奎妥单抗(Talquetamab)为GPRC5D/CD3双特异性抗体。通过与多发性骨髓瘤细胞表面GPRC5D(G蛋白偶联受体C类第5组成员D)和T细胞表面CD3受体结合,引导T细胞定向至多发性骨髓瘤细胞,发挥肿瘤杀伤作用(T细胞重定向治疗)。
此次获批基于单臂、开放标签、多中心1/2期临床试验MonumenTAL-1研究。该研究纳入既往至少接受过3种疗法(包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体)的RRMM患者。研究结果显示,塔奎妥单抗每周0.4mg/kg和每两周0.8mg/kg治疗组总缓解率(ORR)分别为74%和70%。其中59%的患者缓解情况≥VGPR(非常好的部分缓解)。塔奎妥单抗每周和每两周剂量组中位持续应答时间(DOR)分别为9.6个月(95%CI 6.7-13.4)和17.5个月(95%CI 12.5-尚未达到)、中位无进展生存期(mPFS)分别为7.5个月(95%CI 5.7-9.4)和11.2个月(95%CI 8.4-11.6)。
塔奎妥单抗注射液(Talvey)已于2023年8月获得FDA批准用于复发或难治性多发性骨髓瘤。

免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) |
关注“药研苑”公众号,及时掌握最新的药物研发动态。
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。



2024年10月18日,礼新医药其PD-1/VEGF双特异性抗体药LM-299已在中国启动实体瘤1期临床试验。
发布日期:2024-10-18 浏览数:1186

2025年2月11,强生宣布拓立珂®(塔奎妥单抗注射液)获得国家药品监督管理局批准,单药适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38抗体)的成人复发或难…
发布日期:2025-02-11 浏览数:284

2025年1月13日宜明昂科宣布,IMM2510联合化疗治疗一线非小细胞肺癌(NSCLC)的1b/2期临床试验已完成首例患者入组,预计最快在2025年下半年发布该研究的初步临床数据。
发布日期:2025-01-13 浏览数:281

2025年3月10日,辉瑞Pfizer宣布易瑞欧®(埃纳妥单抗)获得国家药品监督管理局附条件批准,用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38单克隆抗体)的复发…
发布日期:2025-03-10 浏览数:263
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3