来源:科伦博泰生物 575
2025年10月21日,科伦博泰生物宣布在2025欧洲肿瘤内科学会(ESMO)年会上公布博度曲妥珠单抗用于接受过≥1种抗HER2治疗(曲妥珠单抗及其生物类似物)和紫杉类治疗的不可切除局部晚期或转移性HER2阳性乳腺癌3期临床试验KL166-Ⅲ-06的研究结果。

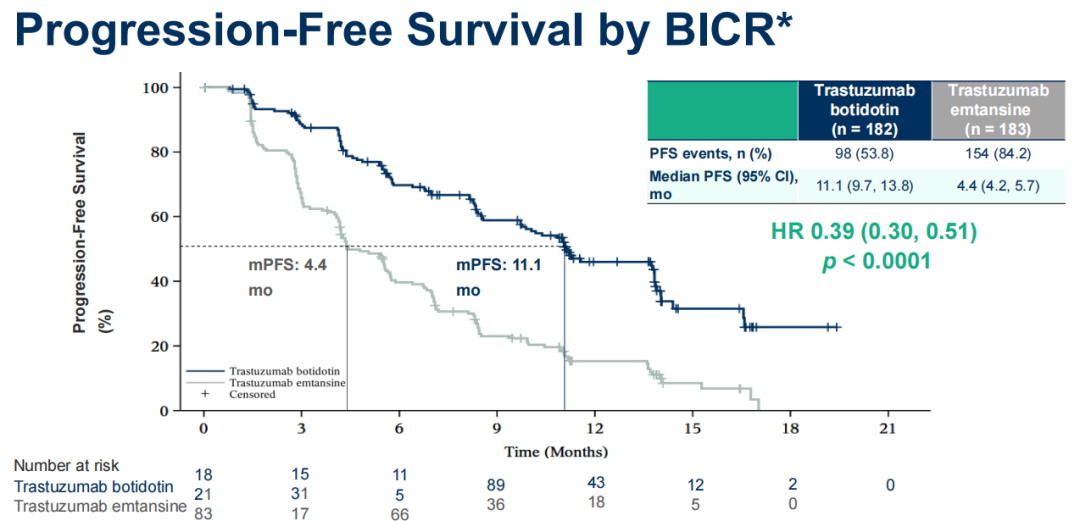
KL166-Ⅲ-06共纳入365名患者,按1:1比例随机接受博度曲妥珠单抗(Trastuzumab Botidotin)4.8mg/kg或恩美曲妥珠单抗(Trastuzumab Emtansine)3.6mg/kg,每3周1次。研究结果显示,博度曲妥珠单抗组中位无进展生存期(PFS)为11.1个月,而恩美曲妥珠单抗组为4.4个月。博度曲妥珠单抗使疾病进展或死亡风险下降61%(HR=0.39,95%CI 0.30-0.51, P < 0.0001)。博度曲妥珠单抗组和恩美曲妥珠单抗组的客观缓解率(ORR)分别为76.9%和53.0%。在安全性方面,博度曲妥珠单抗组最常见的≥3级不良事件(TEAE)为眼部相关不良反应,主要表现为角膜疾病、干眼症和视物模糊等,恩美曲妥珠单抗最常见的≥3级TEAE包括血小板计数降低和中性粒细胞降低等。
博度曲妥珠单抗(A166)为靶向HER2的抗体偶联药物(ADC),有效载荷为微管抑制剂Duostatin-5,属于MMAF(Monomethyl Auristatin F)的衍生物。恩美曲妥珠单抗的有效载荷为微管抑制剂DM1。相关研究显示,搭载MMAF的抗HER2单克隆抗体的抗肿瘤活性强于搭载DM1的抗HER2单克隆抗体(Wen Yin., 2023)。
根据2025年10月17日国家药品监督管理局(NMPA)披露的信息显示,注射用博度曲妥珠单抗(商品名:舒泰莱)已获得国家药品监督管理局批准,用于既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌(NMPA., 2025)。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2024年08月22日,迈威生物Mabwell宣布其向国家药品监督管理局(NMPA)药品审评中心(CDE)递交的关于 “9MW2821 对比研究者选择的化疗治疗含铂化疗失败的复发或转移性宫颈癌的随机、开放、对照、…
发布日期:2024-08-22 浏览数:1500

2025年5月9日,明辉药业宣布与齐鲁制药签订协议,授予齐鲁制药MHB088C(B7-H3 ADC)在大中华区(包括中国大陆、香港、澳门和台湾)的开发、生产和商业化权利。
发布日期:2025-05-09 浏览数:1135

2025年2月11日,科伦博泰宣布将在于2025年美国临床肿瘤学会(ASCO)泌尿生殖系统(GU)癌症研讨会期间公布芦康沙妥珠单抗单药治疗既往接受过抗癌疗法时或治疗后病情进展的不可切除、局部晚期或转…
发布日期:2025-02-11 浏览数:1015

2024年9月30日,康宁杰瑞生物制药宣布其全资子公司江苏康宁杰瑞生物制药有限公司与石药集团全资子公司上海津曼特生物科技有限公司(就康宁杰瑞自主研发的HER2双特异性抗体偶联药物(ADC)JSKN003…
发布日期:2024-09-30 浏览数:969
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3