来源:荃信生物 237
2026年3月9日,荃信生物生物宣布鲁塞奇塔单抗药上市申请(NDA),已于2026年3月9日获得国家药品监督管理局受理,拟定适应症为成人活动性强直性脊柱炎(AS)。

本次申请基于鲁塞奇塔单抗用于成人活动性强直性脊柱炎多中心、随机、双盲、安慰剂对照3期临床试验的研究结果。该试验共纳入641名活动性放射学阳性中轴型脊柱关节炎(强直性脊柱炎)患者。入组患者按1:1比例随机接受鲁塞奇塔单抗160mg皮下注,每4周一次,或安慰剂。至第16周,鲁塞奇塔单抗组达到ASAS40(国际脊柱关节炎协会制定的评估标准改善≥40%)比例为40.4%,显著高于安慰剂组18.9%(P<0.0001)。鲁塞奇塔单抗组和安慰剂组达到ASAS20的比例分别为65.2%和41.3%。在安全性方面,鲁塞奇塔单抗组和安慰剂组治疗期间不良事件的发生率分别为75.8%和71.2%,大多数治疗期间不良事件为1-2级。QX002N组和安慰剂组分别有2.2%和0.9%的患者报告发生严重不良事件(Xiaofeng Zeng., 2025)。
鲁塞奇塔单抗(Crusekitug,研发代号:QX002N)为人源化抗IL-17A单克隆抗体。IL-17A能够引起强效炎症反应。国内已经获批上市的抗IL-17抑制剂类药物包括司库奇尤单抗(Secukinumab)、依奇珠单抗(Ixekizumab )、比奇珠单抗(Bimekizumab)、赛立奇单抗(Xeligekimab)、夫那奇珠单抗(Vunakizumab)和安沐奇塔单抗。比奇珠单抗属于抗IL-17A/F单克隆抗体,其余均为抗IL-17A单克隆抗体
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2025年9月7日,君实生物宣布JS005用于中重度斑块状银屑病,多中心、随机、双盲、平行、安慰剂对照3期临床试验JS005-005-III-PsO研究,达到主要和关键次要研究终点。
发布日期:2025-09-07 浏览数:599
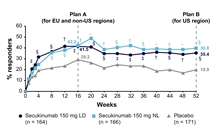
2026年2月3日,诺华宣布可善挺®(司库奇尤单抗)新适应症获得国家药品监督管理局批准,用于对非甾体类抗炎药(NSAID)应答不佳的活动性放射学阴性中轴型脊柱关节炎成人患者。
发布日期:2026-02-03 浏览数:535

2026年2月13日,三生国健宣布安沐奇塔单抗注射液(商品名:益赛拓®)已获国家药品监督管理局批准,用于适合系统治疗或光疗的中度至重度斑块状银屑病成人患者。
发布日期:2026-02-13 浏览数:531

2026年3月11日,优时比UCB宣布在与利生奇珠单抗头对头3期临床试验BE BOLD研究中,比奇珠单抗至第16周,在改善活动性银屑病关节炎(PsA)ACR50(PsA疾病体征和症状至少改善50%)方面,取得统计学…
发布日期:2026-03-11 浏览数:262
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3