来源:优时比 5
2026年3月27日优时比UCB宣布,比奇珠单抗(倍捷乐®)已获得中国国家药品监督管理局(NMPA)批准,用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者,以及治疗常规系统性治疗疗效不佳的中度至重度化脓性汗腺炎(反常性痤疮)成人患者。

在BE VIVID、BE SURE、BE READY等研究中,验证了比奇珠单抗治疗中重度斑块状银屑病(PsO)的有效性和安全性。
BE READY为多中心、随机、双盲、安慰剂对照组3a期临床试验,共纳入435名中重度斑块银屑病患者。入组患者按4:1比例随机接受比奇珠单抗(320mg每四周一次)、或安慰剂。至第16周,比奇珠单抗组和安慰剂组达到皮损清除或几乎清除(PASI 90)的比例分别为91%、1%(P<0.0001),达到皮肤光洁或几乎光洁(IGA分级为0或1)的比例分别为93%和1%(P<0.0001)(Kenneth B Gordon., 2021)。
BE VIVID为多中心、双盲、阳性对照组和安慰剂对照3a期临床试验,共纳入567名中重度斑块状银屑病患者。入组患者按4:2:1比例随机接受比奇珠单抗(320mg每四周一次)、乌司奴单抗(Ustekinumab,抗IL-23/IL-12单克隆抗体;45mg或90 mg第0、4周,之后每十二周一次),或安慰剂。至第16周,比奇珠单抗组、乌司奴单抗组和安慰剂组达到PASI 90的比例分别为85%、50%和5%(p均<0.0001)。上述各组达到达到IGA分级为0或1的比例分别为84%、53%和5%(p均<0.0001)(Kristian Reich., 2021)。
BE SURE为多中心、随机、双盲、阳性对照组3a期临床试验,共纳入478名中重度斑块银屑病患者。入组患者按1:1:1比例随机接受比奇珠单抗(320mg每四周一次)、比奇珠单抗(320mg每四周一次至第16周,之后每八周一次)、或阿达木单抗(Adalimumab,抗TNF-α单克隆抗体;40mg每两周一次至第24周,之后转为比奇珠单抗320mg每四周一次)。至第16周,比奇珠单抗组和阿达木单抗组达到PASI 90的比例分别为86.2%和47.2%(P<0.001),达到IGA分级为0或1的比例分别为85.3%和57.2%(P<0.001)(Richard B Warren., 2021)。
BE BRIGHT为上述三项临床试验开放标签延长期(OLE)研究结果,至第52周达到皮肤光洁(PASI 100)的比例为76.2%,至第196周为64.7%(Andrew Blauvelt., 2025)。
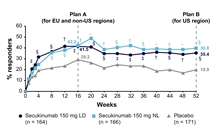
BE RADIANT多中心、随机、双盲、阳性对照组3b期临床试验,共纳入743名中重度斑块银屑病患者。入组患者按1:1比例随机接受比奇珠单抗(320mg每四周一次至16周,之后按1:2比例随机转为每四周一次或每八周一次)、或司库奇尤单抗(Secukinumab,抗IL-17A单克隆抗体;300mg每周一次至第4周,之后每四周一次)。至第16周,比奇珠单抗组和司库奇尤单抗组达到PASI 100的比例分别为61.7%和48.9%(P<0.001)。至第48周,比奇珠单抗组和司库奇尤单抗组达到PASI 100的比例分别为67.0%和46.2%(P<0.001)(Kristian Reich., 2021)。
在BE HEARD I、II及BE HEARD EXT研究中验证了比奇珠单抗治疗中重度化脓性汗腺炎的有效性和安全性。
BE HEARD I和II为两项设计相同的多中心,随机、双盲、安慰剂对照3三期临床试验,共纳入1014名患者,入组患者按2:2:2:1比例随机接受比奇珠单抗(320mg每两周一次)、比奇珠单抗(320mg每两周一次至第16周,之后每四周一次)、比奇珠单抗(320mg每四周一次)、或安慰剂(至第16周,之后转为比奇珠单抗320mg每两周一次)。至第16周,在BE HEARD I研究中比奇珠单抗每两周一次组和安慰剂组达到HiSCR 50(化脓性汗腺炎体征和症状达到50%或更大幅度)的比例分别为48%和29%(p=0.0060),在BE HEARD II研究中分别为52%和32%(p=0.0032)。BE HEARD II研究,比奇珠单抗每四周一次组也达到了治疗终点,达到HiSCR50的比例为54%(p=0.0038)(Alexa B Kimball., 2024)。
BE HEARD EXT为BE HEARD I和II的开放标签延长期试验,在BE HEARD I和II研究中完成48周试验的患者进入BE HEARD EXT研究。至第3年接受比奇珠单抗长期间治疗的患者达到HiSCR 90和HiSCR 100的比例分别为74.1%和62.1%(UCB., 2026)。
在安全性方面,比奇珠单抗盲法和开放标签临床研究中,最常报告的不良反应为上呼吸道感染和口腔念珠菌病。斑块状银屑病3期临床试验安慰剂对照阶段,至第16周,比奇珠单抗组和安慰剂组分别有36.0%和22.5%的患者报告发生感染。大多数感染为轻中度上呼吸道感染,比奇珠单抗组和安慰剂组严重感染的发生率分别为0.3%和0%。比奇珠单抗组口腔和口咽念珠菌病发生率分别为7.3%和1.2%,安慰剂组为0%,98%以上的患者为非严重病例,无需终止治疗。在斑块状银屑病3期临床试验的整个治疗期间,比奇珠单组感染的发生率为63.2%,严重感染的发生率为1.5%。在化脓性汗腺炎3期临床试验中,比奇珠单组的感染率与在其他适应症中观察到的数值相似。在安慰剂对照阶段,比奇珠单抗组口腔和口咽念珠菌病的发生率分别为7.1%和0%,安慰剂组为0%。
比奇珠单抗(Bimekizumab)为抗IL-17A/IL-17F单克隆抗体。IL-17家族包括6个成员,IL-17A、IL-17B、IL-17C、IL-17D、IL-17E (IL-25)和IL-17F。IL-17F与IL-17A序列存在55%的同源性,结构相似,可形成异源二聚体。IL-17家族不同成员对于炎症的影响并不相同,IL-17A能够引起强效炎症反应。IL-17抑制剂类药物目前已经被准用于多种自身免疫性疾病。除上述适应症之外,比奇珠单抗(倍捷乐®)已在中国获批用于常规治疗疗效不佳或不耐受的活动性强直性脊柱炎(AS)成人患者;及用于非甾体类抗炎药(NSAID)给药后疗效不佳或不耐受的活动性放射学阴性中轴型脊柱关节炎(nr-axSpA)伴客观炎症体征(根据C反应蛋白(CRP)升高和/或磁共振成像(MRI)检查提示)的成人患者。

免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2025年9月7日,君实生物宣布JS005用于中重度斑块状银屑病,多中心、随机、双盲、平行、安慰剂对照3期临床试验JS005-005-III-PsO研究,达到主要和关键次要研究终点。
发布日期:2025-09-07 浏览数:451
2026年2月3日,诺华宣布可善挺®(司库奇尤单抗)新适应症获得国家药品监督管理局批准,用于对非甾体类抗炎药(NSAID)应答不佳的活动性放射学阴性中轴型脊柱关节炎成人患者。
发布日期:2026-02-03 浏览数:284

2026年2月13日,三生国健宣布安沐奇塔单抗注射液(商品名:益赛拓®)已获国家药品监督管理局批准,用于适合系统治疗或光疗的中度至重度斑块状银屑病成人患者。
发布日期:2026-02-13 浏览数:238

2026年3月9日,荃信生物生物宣布鲁塞奇塔单抗药上市申请(NDA),已于2026年3月9日获得国家药品监督管理局受理,拟定适应症为成人活动性强直性脊柱炎(AS)。
发布日期:2026-03-09 浏览数:92
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3