来源:Eli Lilly 1311
2024年7月2日,礼来公司宣布FDA批准Donanemab(商品名Kisunla™)350 mg/20 mL,每月一次静脉输注用于治疗处于轻度痴呆阶段,伴有轻度认知障碍(MCI),并经淀粉样蛋白病理学确诊的成人早期症状性阿尔茨海默病(AD)。

Donanemab属于靶向β淀粉样蛋白斑块的单克隆抗体。每四周静脉注射一次,前三剂700mg/次,之后1400mg/次。

3期临床试验TRAILBLAZER-ALZ 2(NCT04437511)显示,对于轻中度tau蛋白病理表现患者Donanemab组《整合阿尔茨海默病量表(iADRS)》评分下降与对照组相比减少35%。在全部受试者中Donanemab组iADRS评分下降与对照组相比减少22%。与安慰剂相比,接受Donanemab治疗的患进展到下一个临床阶段疾病的风险降低了39%。与研究开始时相比,Donanemab在第6个月时β淀粉样斑块平均61% ,第在12 月时减少80%,第18个月时减少了84%。
Donanemab可引起β淀粉样蛋白相关成像异常 (ARIA),属于靶向β淀粉样斑块疗法的潜在副作用,通常不会引起症状。它可以通过磁共振成像 (MRI) 扫描进行检测。可表现为大脑一个或多个区域出现暂时性肿胀,肿胀通常会随着时间的推移而消退。也可能表现为大脑内或表面出现小的出血点。在极少数情况下,脑部可能会出现大面积的出血。
免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。


2024年10月29日,礼来Eli Lilly宣布Donanemab(商品名:Kisunla)TRAILBLAZER-ALZ 6研究3b期临床试验取得积极结果。
发布日期:2024-10-29 浏览数:1567
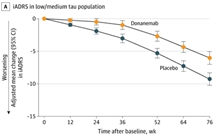
2023年7月17日Eli Lilly公布了抗β淀粉样蛋白(Aβ)单克隆抗体Donanemab的3期临床试验TRAILBLAZER-ALZ 2试验结果。试验显示 Donanemab能够有效改善Aβ斑块检测阳性阿尔茨海默症早期症状患者的认…
发布日期:2023-07-17 浏览数:1509

2024年7月2日,礼来公司宣布FDA批准Donanemab(商品名Kisunla™)350 mg/20 mL,每月一次静脉输注用于治疗处于轻度痴呆阶段,伴有轻度认知障碍(MCI),并经淀粉样蛋白病理学确诊的成人早期症状性…
发布日期:2024-07-02 浏览数:1310
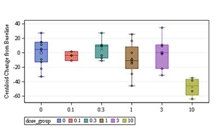
Intravenous donanemab 10 mg/kg can reduce amyloid deposits in AD despite having a shorter than expected half-life.
发布日期:2021-02-14 浏览数:1224
 改变滴定方案礼来降低其阿尔茨海默症抗体药物脑水肿发生率
改变滴定方案礼来降低其阿尔茨海默症抗体药物脑水肿发生率横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3