来源:礼来Eli Lilly 2825
2024年7月19日,礼来Eli Lilly在其公众号上宣布其替尔泊肽制剂穆峰达(替尔泊肽注射液)获得国家药品监督管理局批准用于在控制饮食和增加运动基础上,体重指数(BMI)符合以下要求的成人的长期体重管理:≥28 kg/m2(肥胖),或≥24 kg/m2(超重)并伴有至少一种体重相关合并症(如:高血压、血脂异常、高血糖、阻塞性睡眠呼吸暂停、心血管疾病等)。

替尔泊肽是GIP(葡萄糖依赖性促胰岛素多肽)和GLP-1(胰高血糖素样肽-1)双受体激动剂。通过激动GIP受体和GLP-1受体,抑制食欲,减少食物摄入、降低体重和减少脂肪。其还能够降低空腹和餐后血糖。2024年5月获得家药品监督管理局批准替尔泊肽在饮食控制和运动基础上,用于接受二甲双胍和/或磺脲类药物治疗血糖仍控制不佳的成人2型糖尿病患者。
本次批准,主要基于在中国进行的3期临床试验SURMOUNT-CN的研究结果。 SURMOUNT-CN是一项多中心、随机、双盲、平行、安慰剂对照3期临床试验,共纳入210名肥胖(BMI≥28 kg/m2)或伴有至少一种合并症的超重(BMI≥24 kg/m2)中国成人受试者。受试者按1:1:1的比例随机分组,分别接受替尔泊肽10 mg、15 mg或安慰剂每周一次进行治疗。至第52周,替尔泊肽10mg组和15mg组平均体重较基线分别降低14.4%和19.9%,均优于安慰剂组(降低2.4%)。替尔泊肽10mg组和15mg组达到体重减轻≥5%的受试者比例分别为91.4%和92.7%,优于安慰剂组(29.4%)。替尔泊肽10mg组和15mg组平均腰围较基线分别减少11.9 cm和16.4cm,优于安慰剂(减少2.7cm)。
在SURMOUNT-CN试验中替尔泊肽在治疗期间出现不良事件与先前试验报道相似,未发现新的安全性信号。替尔泊肽组最常报告的治疗期间不良事件为胃肠道不良事件,其严重程度大多为轻度至中度,主要发生在剂量递增期间。

免责声明:相关信息仅限药物研发参考使用,本网站不保证信息真实和准确!
关注“药研苑”公众号,查看前景解析。

|
推荐阅读: ・2025年1-3季度口崩片市场哪个强? ・2025年1-3季度口溶膜制剂哪家强? ・免疫检查点抑制剂,谁将成为下一个王者? ・质子泵相关抑酸类药物市场即将回暖 ・中药1类新药距离封神还有多远 |
|
“药品营销避坑”试读: ・药品立项需要注意什么(一) ・药品生命周期管理(一) ・改剂型,口服液体制剂“金矿”还是“陷阱 |
我们提供如下咨询服务:药品信息发布、药品立项、市场前景分析、医院及药品零售市场分析、药品市场调研及制定推广策略、国外药品引进、国内批文转让、上市前后临床试验设计、药品彩页及主图设计、药品推广PPT制作。您可以关注公众号“药研苑”后,在主页面发送消息,咨询相关服务。

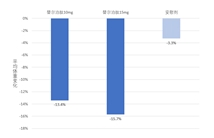
2023年4月27日礼来(Eli Lilly)公司公布了替尔泊肽(Tirzepatide)SURMOUNT-2临床试验的结果。经过72周的治疗,10mg替尔泊肽剂量组的平均减重幅度达到13.4%,15mg替尔泊肽剂量的平均减重幅度达到…
发布日期:2023-04-27 浏览数:3108
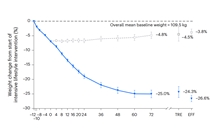
替尔泊肽(Tirzepatide)SURMOUNT-3临床试显示,12周严格生活干预加72周替尔泊肽,共实现减重26.6%。
发布日期:2023-07-27 浏览数:3011

2023年11月8日礼来Eli Lilly在线宣布其GIP/GLP-1双受体激动剂类药物替尔泊肽(Zepbound)获得美国FDA批准用于BMI≥30的肥胖患者或BMI≥27 并伴有与体重相关疾病的超重患者。
发布日期:2023-11-08 浏览数:2950

2024年7月19日,礼来Eli Lilly在其公众号上宣布其替尔泊肽制剂穆峰达(替尔泊肽注射液)获得国家药品监督管理局批准用于在控制饮食和增加运动基础上,体重指数(BMI)符合以下要求的成人的长期体…
发布日期:2024-07-19 浏览数:2824
横切线®为注册商标
Copyright 2020 横切线®药研苑 备案号:粤ICP备18041379号-3